-
外泌体 编辑
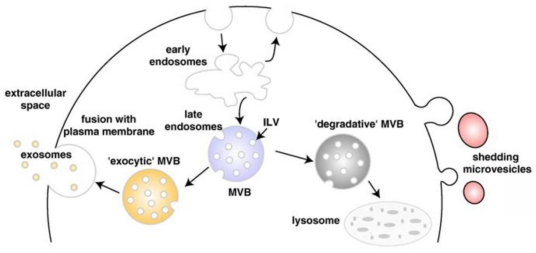
1983年,外泌体首次于绵羊网织红细胞中被发现, 1987年Johnstone将其命名为“exosome”。现今,其特指直径在40-100nm的盘状囊泡。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中 。
外泌体富含胆固醇和鞘磷脂。2007年, Valadi等发现鼠的肥大细胞分泌 的 exosome可以被人的肥大细胞捕获,并且其携带的mRNA成分可以进入细胞浆中可以被翻译成蛋白质,不仅仅是mRNA,exosomes所转移的microRNA同样具有生物活性,在进入靶细胞后可以靶向调节细胞中mRNA的水平。这一发现使得研究人员对exosome的研究热情激增,截止已经通过286项研究发现了41860种蛋白质、2838种microRNA、3408种mRNA。
一类外泌体中常见的细胞质蛋白是Rabs蛋白,是鸟苷酸三磷酸酶(GTPases,)家族的一种。它可以调节外泌体膜与受体细胞的融合,有文献报道称RAB4, RAB5和 RAB11主要出现于早期以及回收的核内体中,RAB7 和 RAB9主要出现于晚期的核内体。现有大量的研究发现外泌体中含有40种RAB蛋白。除了RAB蛋白,外泌体中富含具有外泌体膜交换以及融合作用的膜联蛋白(包括膜联蛋白1、2、4、5、6、7、11等)。外泌体膜上富含参与外泌体运输的四跨膜蛋白家族(CD63, CD81 和CD9)、热休克蛋白家族((HSP60, HSP70, HSPA5, CCT2 和HSP90以及一些细胞特异性的蛋白包括A33(结肠上皮细胞来源)、MHC-Ⅱ(抗原提呈细胞来源)、CD86(抗原提呈细胞来源)以及乳凝集素(不成熟的树突状细胞)。其它一些外泌体中的蛋白包括多种的代谢类的酶(GAPDH, 烯醇化酶 1, 醛缩酶 1, PKM2, PGK1, PDIA3, GSTP1,DPP4, AHCY, TPL1, 抗氧化蛋白, P4HB, LDH, 亲环素 A,FASN, MDH1 和CNP)、核糖体蛋白(RPS3)、信号转导因子(黑色素瘤分化相关因子, ARF1, CDC42, 人类红细胞膜整合蛋白, SLC9A3R1)、粘附因子(MFGE8、整合素)、细胞骨架蛋白以及泛素等。
外泌体的提取主要包括以下几种方式。
一是超速离心法,这是外泌体提取最常用的方法 。此种方法得到的外泌体量多,但是纯度不足,电镜鉴定时发现外泌体聚集成块, 由于微泡和外泌体没有非常统一的鉴定标准,也有一些研究认为此种 方法得到的是微泡不是外泌体 。
二是过滤离心, 这种操作简单、省时,不影响外泌体的生物活性 ,但同样存在纯度不足的问题。
三是密度梯度离心法, 用此种方法分离到 的外泌体纯度 高,但是前期准备工作繁杂,耗时,量少。
四是免疫磁珠法,这种方法可以保证外泌体形态 的完整,特异性高、操作简单、不需要昂贵的仪器设备,但是非中性pH 和非 生理性盐浓度会影响外泌体生物活性, 不便进行下一步的实验 。
五是PS亲和法,该方法将PS(磷脂酰丝氨酸)与磁珠结合,利用亲和原理捕获外泌体囊泡外的PS。该方法与免疫磁珠法相似,获得的外泌体形态完整,纯度最高。由于不使用变性剂,不影响外泌体的生物活性,外泌体可用于细胞共培养和体内注射。2016.9 《Scientific Reports》 杂志发表了该方法最新数据,表明PS法可提取相当高纯度的外泌体。
六是色谱法,这种方法分离到的外泌体在 电镜下大小均 一, 但是需要特殊的设备 , 应用不广泛 。
七是微流控分离法,该方法通过负压及震荡等机械原理分离外泌体,产量纯度均具有较大幅度提高,但需要特定设备配合。
人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而激活靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而激活细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA。
当外泌体在1983年首次被发现后,其被认为是细胞排泄废物的一种方式,如今随着大量对其生物来源、其物质构成及运输、细胞间信号的传导以及在体液中的分布的研究发现外泌体具有多种多样的功能。外泌体的功能取决于其所来源的细胞类型,其可参与到机体免疫应答、抗原提呈、细胞迁移、细胞分化、肿瘤侵袭等方方面面。有研究表明肿瘤来源的外泌体参与到肿瘤细胞与基底细胞的遗传信息的交换,从而导致大量新生血管的生成,促进了肿瘤的生长与侵袭。
1. Suresh Mathivanan, Hong Ji, Richard J. Simpsonet al. Exosomes: extracellular organelles important in interCELLular communication Journal of proteomics 7 3 ( 2010 ) 1907 – 1920
2. Richard J Simpson†,Justin WE Lim,RobERT L Moritz andSuresh Mathivanan et al. E xosomes: proteomic insightsand diagNOstic potential. Expert Rev. Proteomics 6(3), 267–283 (2009)
3. 卢婉, 杨人强, 王伶. 外泌体的研究进展.生命的化学 ,2013,33( 4):438.442
4. 李栋,邱丽华. 外泌体及其在卵巢癌中的研究进展. 理 妇产科进展 2014 年 7 月第 23 卷第 7 期 Prog Obstet Gynecol,Ju1.2014,Vo1.23,No.7
5. 简 雯,李 剑,涂军木. 微泡的产生机制、生物学功能及应用前景. 生命的化学,2014, 34(5):686— 689
6. Hadi Valadi, Karin Ekström1, Apostolos Bossios, Margareta Sjöstrand1, James J. Lee and Jan O. Lötvall et al. Exosome-mediated transfer of mRNAs and microRNAs is a novel mechanism of genetic exchAnge between cells. Nat Cell Biol 2007;9:654–9.
7. Andersen JS, Mann M. Organellar proteomics: tuRNIng inventories into insights. EMBO Rep 2006;7:874–9.
8. Piccin A, Murphy WG, Smith OP. Circulating microparticles:pathophysiology and clinical implications. Blood Rev 2007;21:157–71.
9. del Conde I, Shrimpton CN, Thiagarajan P, Lopez JA.tissue-factor-bearing microvesicles arise from lipid rafts and fuse with activated platelets to initiate coagulation.Blood 2005;106:1604–11.
10. Ratajczak J, Wysoczynski M, Hayek F, Janowska-Wieczorek A,Ratajczak MZ. Membrane-derived microvesicles: important and underappreciated mediators of cell-to-cell communication.Leukemia 2006;20:1487–95.
11. Mears R, Craven RA, Hanrahan S, Totty N, Upton C, Young SL,Patel P, Selby PJ, Banks RE. Proteomic analysis of melanomaderived exosomes by two-dimensional polyacrylamide gel elECTrophoresis and mass SPECTrometry. Proteomics 2004;4:
4019–31.