-
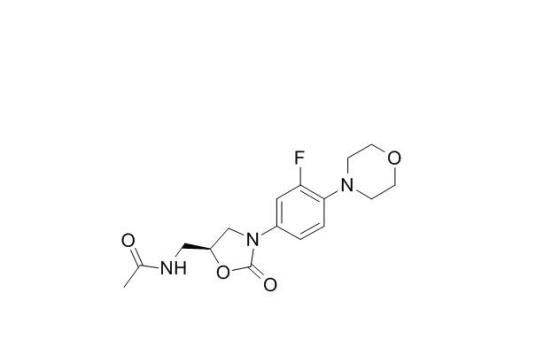
雷奈佐利 编辑
中文名:雷奈佐利
外文名:linezolid
别名:吗啉恶酮
分子量:337.3461
CAS登录号:165800-03-3
沸点:585.5°Cat760mmHg
密度:1.302g/cm3
闪点:307.9°C
(s)-n-methyl]acetamide; Linezolid & its intermediates(R&D); N-({(5R)-3--2-oxo-1,3-oxazolidin-5-yl}methyl)acetamide; N-({(5S)-3--2-oxo-1,3-oxazolidin-5-yl}methyl)acetamide
1.将乙酸乙酯、吗啉和二异丙基乙基胺混合,搅拌下滴加3,4-二氟硝基苯,反应完毕后。用乙酸乙酯萃取,饱和盐水洗涤,干燥,蒸干,丙酮-水重结晶,得3-氟-4-吗啉基硝基苯。将还原铁粉、水和冰乙酸混合,回流一定时间,滴加3-氟-4-吗啉基硝基苯的无水乙醇溶液,反应完毕后,趁热过滤,蒸干,得到的物质用乙酸乙酯萃取,盐水洗涤,干燥,蒸干,得3-氟-4-吗啉基苯胺。将其溶于丙酮和水的混合溶液中,加入碳酸氢钠,滴加氯甲酸甲酯,搅拌,抽滤,得固体,滤液放入冰水,抽滤得到固体。所得固体用丙酮?水重结晶,得苄氧羰基-3-氟-4-吗啉基苯胺。将其溶于无水四氢呋喃,在氨气保护下,滴加丁基锂溶液,再滴(R)-缩甘油丁酯,反应后,加入饱和氯化铵溶液、乙酸乙酯、水。用乙酸乙酯萃取,饱和盐水洗,干燥,蒸干,将得到的物质溶于二氯甲烷和三乙胺中,滴加甲磺酰氯进行反应。用二氯甲烷萃取,用饱和盐水洗,干燥,蒸干,得磺酸酯。将磺酸酯和叠氮化<br钠溶于二甲基甲酰胺反应。用乙酸乙醇萃取,饱和盐水洗,干燥,蒸干,取代得叠氮衍生物。将该衍生物和5%钯?碳在无水乙醇中反应一定间,过滤,蒸干,得到的物质溶于四氢呋喃和氢氧化钠水溶液中,加入乙酸酐,用乙酸乙酯萃取,饱和盐水洗,干燥。蒸干,硅胶柱层析,乙酸乙酯-正己烷重结晶,即得利奈唑胺。
2. ®-(3-间氟苯基-2-氧代-5-唑烷基)氯甲烷的制备在反应瓶中加入无水溴化锂0.5g(5.8mmol)、三正丁基氧磷1.26g(5.8mmol) 和甲苯40ml, 加热搅拌回流共沸分出水(通过分水器进行)1h. 冷却, 滴入间氟苯基异氰酸酯13.7g(0.1mol) 和 ®-环氧氯丙烷9.2g(0.1mol) 的甲苯70ml溶液, 保持微沸, 滴毕, 再回流搅拌2h. 减压蒸除溶剂, 剩余物中加入乙醚20ml, 析出固体, 过滤, 滤饼用乙醚洗, 抽干, 干燥, 得 ®-(3-间氟苯基-2-氧代-5-唑烷基) 氯甲烷19, 收率83%,mp88.0~89.0 ºC (甲苯).
3.3-间氟苯基-2-氧代-5-唑烷基)叠氮甲烷的制备在反应瓶中加入 ®-(3-间氟苯基-2-氧代-5-唑烷基)氯甲烷19g(8.3mmol)、叠氮化钠10.8g(166mmol) 、碘化钠0.6g(4.5mmol) 和DMF100ml, 于80 ºC搅拌反应4h. 冷却, 倒至300ml水中, 乙酸乙酯提取, 水洗, 无水硫酸镁干燥, 过滤, 滤液蒸干溶剂, 得白色固体 ®-(3-间氟苯基-2-氧代-5-唑烷基) 叠氮甲烷18.3g, 收率93.8%,mp130~132 ºC
4. ®-(3-间氟苯基-2-氧代-5-唑烷基)甲基乙酰胺的制备在反应器中加入 ®-(3-间氟苯基-2-氧代-5-唑烷基)叠氮甲烷18.3g(78mmol) 、乙酸乙酯200ml、10%(质量分数)Pd/C0.4g. 将该氢化反应器用N2排除空气, 充氢气置换N2后, 充氢气压力为1.05×105, 室温下搅拌反应10h. 过滤, 滤液中加入三乙胺12.5ml(90mmol), 冷至0 ºC, 滴加乙酸酐22ml(0.234mol), 滴毕, 室温搅拌30min. 减压浓缩至浓, 冷却析出固体, 过滤, 甲醇水溶液洗滤饼, 抽干, 干燥, 得白色固体16.9g, 收率86%,mp135~136 ºC.
5. ®-甲基乙酰胺的制备在反应瓶中加入 ®-(3-间氟苯基-2-氧代-5-唑烷基)甲基乙酰胺16.9g(67mmol)、冰醋酸100ml, 搅拌溶解, 再加入钨酸钠3.0g(11mmol) 和溴化钾9g(76mmol)的50ml水溶液. 在另一反应瓶中加入冰醋酸350ml、乙酸酐100ml、浓硫酸25ml, 冰浴冷却下再在搅拌下慢慢加入过硼酸钠28g(0.34mol), 搅拌10min, 所得的溶液于室温下滴入上述加有 ®-(3-间氟苯基-2-氧代-5-唑烷基)甲基乙酰胺的反应瓶中, 的反应瓶中30min滴完. 升温至75 ºC. 搅拌2h. 减压浓缩至约100ml, 倒入200ml水中,乙醚提取,有机层用无水硫酸镁干燥,过滤,滤蒸发至干,得白色固体19g, 收率86%,mp156~157 ºC.
6. 利奈唑酮的合成在反应瓶中加入 ®-甲基乙酰胺19g(57mmol) 、吗啉10.5g(0.12mol) 、碘化亚铜1.1g(6mmol) 、L-脯氨酸0.7g(6mmol) 和DMF200ml, 于90 ºC搅拌反24h. 减压浓缩至干, 加入乙酸乙酯200ml, 过滤, 滤液用0.36mol/L碳酸钾水溶液洗, 饱和NaCL溶液洗,蒸馏水洗,无水硫酸镁干燥,蒸发至干,用乙酸乙酯/石油醚重结晶,得白色固体利奈唑酮14.4g, 收率75%,mp182~183 ºC