-
自发反应 编辑
化学热力学指出,熵增加,焓减小的反应必定是自发反应。自发反应不一定是快速反应。
如无钯作催化剂常温常压下氢氧混合气可长期保持无明显反应。在同等条件下,自发反应的逆反应都是非自发的,须给予外力对之作功才能进行。
△G=△H-T△S
△G——吉布斯自由能变
△H——焓变(△H<0为放热反应,△H>0为吸热反应)
△S——熵变(物质混乱度的量度,如固体变成气体或气体体积增大,则混乱度增加,△S>0)
T——开氏温度(永远不可能为负值) 判断反应能否自发进行用吉布斯自由能判据。
如果△G<0 反应可以自发进行;反之则不可以自发进行。
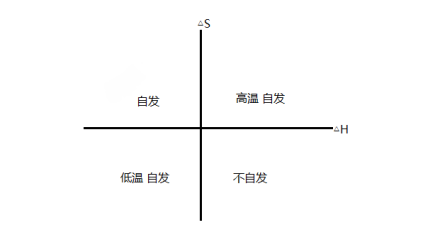
恒温恒压下:当△H<0,△S>0时,反应自发进行;
当△H>0,△S<0时,反应不自发进行;
当△H>0,△S>0时,需要在较高温度的条件下,才能自发进行。
当△H<0,△S<0时,需要在较低温度的条件下,才能自发进行。
一般低温时焓变影响为主;高温时,熵变影响为主,而温度影响的大小要看△H和△S的具体数值而定。
反应总是在一定条件下进行的。要讨论反应的自发性,也要指明反应条件。如果没有交代反应条件,只讲“某某反应不自发”“某某反应自发”,实际上是指在常温常压下进行的反应。“一定条件”指“一定的温度一定压强”。例如,反应 CaCO3== CaO + CO2↑ 在常温常压是非自发的,而在高温下则是自发发生的。 用吉布提自由能计算公式(△G=△H-T△S)来判断反应能否自发进行时,可以看到T对△G的值有影响,在某些情况下,可能决定△G是大于0还是小于0;式中△H 是一个与温度、压强有关的物理量。因此,讨论△G是大于0还是小于0,实际上也是在一定温度与压强下进行的。
“外界帮助”这句话中,指的是为反应体系提供能量。“帮助”并不是指提供反应发生的温度和压强等反应条件,也不是点燃、使用催化剂等等。一定的温度、一定的压强是反应所需要的条件。很多场合下,提高温度,往往是为了加速反应。合成氨反应在常温常压下,△G<0,是放热的自发反应。但是,常温常压下实际上无法觉察到反应的发生,只有在高温、高压、催化剂存在下,才有实际的应用价值。又如,硝酸铵NH4NO3的分解反应, △H<0 △S>0,在任何温度下都能自发进行。在常温常压下,反应速率慢,难以观察到反应的发生。但加热到高温,或受猛烈撞击,发生爆炸性分解:2NH4NO3=N2↑+O2↑+4H2O。撞击或加热大大提高反应速率,发生剧烈分解。氢气氧气化合成水的反应在常温下也是自发的。常温下将H2与O2混合,不能观察到有明显现象,在氢氧燃料电池中,反应在常温下就能进行。在钯粉催化下H2与O2的混合气体也能快速生成水。点燃氢气氧气,能迅速化合成水,也只是加速了反应速率。
从热力学分析,“外界帮助”指的是对体系做“有用功”。例如,水的分解在常温常压下是不自发的,但通电,为体系提供电能,可以使水分解成H2和O2 。电解反应都是非自发反应,“通电”对体系做有用功,使反应在常温常压下得以进行。而原电池反应是自发反应,它能对外作电功。自发反应和其他自发过程一样,具有对外作功的能力。因此,自发反应和非自发反应的区别在于在一定条件下,反应的发生是需要外界对体系作功,还是反应体系具有能对外界作功的能力。