-
β-内酰胺 编辑
此类抗生素具有杀菌活性强、毒性低、适应症广及临床疗效好的优点。本类药化学结构,特别是侧链的改变形成了许多不同抗菌谱和抗菌作用以及各种临床药理学特性的抗生素。
(一)抗菌作用机制
各种β-内酰胺类抗生素的作用机制均相似,都能抑制胞壁粘肽合成酶,即青霉素结合蛋白从而阻碍细胞壁粘肽合成,使细菌胞壁缺损,菌体膨胀裂解(胞壁粘肽合成过程见三十七章)。除此之外,对细菌的致死效应还应包括触发细菌的自溶酶活性,缺乏自溶酶的突变株则表现出耐药性。哺乳动物无细胞壁,不受β-内酰胺类药物的影响,因而本类药具有对细菌的选择性杀菌作用,对宿主毒性小。近十多年来已证实细菌细胞膜上特殊蛋白PBPs(青霉素结合蛋白)是β-内酰胺类药的作用靶位,PBPs的功能及与抗生素结合情况归纳于图38-1。各种细菌细胞膜上的PBPs数目、分子量、对β-内酰胺类抗生素的敏感性不同,但分类学上相近的细菌,其PBPs类型及生理功能则相似。例如大肠杆菌有7种PBPs,PBP1A,PBP1B与细菌延长有关,青霉素、氨苄西林、头孢噻吩等与PBP1A、PBP1B有高度亲和力,可使细菌生长繁殖和延伸受抑制,并溶解死亡,PBP2与细管形状有关,美西林、棒酸与硫霉素(亚胺培南)能选择性地与其结合,使细菌形成大圆形细胞,对渗透压稳定,可继续生几代后才溶解死亡。PBP3功能与PBP1A相同,但量少,与中隔形成,细菌分裂有关,多数青霉素类或头孢菌素类抗生素主要与PBP1和(或)PBP3结合,形成丝状体和球形体,使细菌发生变形萎缩,逐渐溶解死亡。PBP1,2,3是细菌存活、生长繁殖所必需,PBP4,5,6;与羧肽酶活性有关,对细菌生存繁殖无重要性,抗生素与之结合后,对细菌无影响。
(二)影响β-内酰胺类抗菌作用素
革兰阳性菌与阴性菌的结构差异甚大,β-内酰胺类各药与母核相联接的侧链不同可影响其亲脂性或亲水性。有效药物必需能进入菌体作用于细胞膜上的靶位PBPs。影响抗菌作用的主要因素:①药物透过革兰阳性菌细胞壁或阴性菌脂蛋白外膜(即第一道穿透屏障)的难易;②对β-内酰胺酶(第二道酶水解屏障)的稳定性;③对抗菌作用靶位PBPs的亲和性。根据这些因素,目前临床应用的β-内酰胺类对革兰阳性与阴性菌的作用大致有6种类型:Ⅰ类为青霉素及口服青霉素V易透过革兰阳性菌胞壁粘肽层,但它们不能透过革兰阴性菌糖蛋白磷脂外膜,因而属窄谱的仅对革兰阳性菌有效。Ⅱ类包括有氨苄西林、羧苄西林、酰脲类青霉素、亚胺培南及若干头孢菌素,能适度透过革兰阳性菌的胞壁粘肽层,对革兰阴性菌的外膜透过性则很好,因而是广谱抗菌药物。Ⅲ类为青霉素等容易被革兰阳性菌的胞外β-内酰胺酶即青霉素酶破坏灭活的青霉素类,对产酶菌往往表现明显的耐药性。Ⅳ类为异恶唑类青霉素、头孢菌素一、二代及亚胺培南等对青霉素酶稳定,对革兰阳性的产酶菌有效,但对染色体突变而改变的PBPs结构,可使药物与PBPs的亲和力下降或消失,因而无效。Ⅴ类包括酰脲类青霉素(阿洛西林与美洛西林等)、羧苄青霉素及头孢菌素一、二代,当胞膜外间隙的β-内酰胺酶少量存在时有抗菌效果,大量酶存在时,则被破坏而无效。Ⅵ类包括第三代头孢菌素、氨曲南、亚胺培南等对β-内酰胺酶十分稳定,即使大量β-内酰胺酶存在时仍然有效,但对因染色体突变而改变了的PBPs则无效,加用氨基甙类抗生素也仍然无效。
(三)细菌耐药机制
细菌对β-内酰胺类抗生素耐药机制可概括为:①细菌产生β-内酰胺酶(青霉素酶、头孢菌素酶等)使易感抗生素水解而灭活;②对革兰阴性菌产生的β-内酰胺酶稳定的广谱青霉素和第二、三代头孢菌素,其耐药发生机制不是由于抗生素被β-内酰胺酶水解,而是由于抗生素与大量的β-内酰胺酶迅速、牢固结合,使其停留于胞膜外间隙中,因而不能进入靶位(PBPs)发生抗菌作用。此种β-内酰胺酶的非水解机制又称为“牵制机制”(trapping mechanism);③PBPs靶蛋白与抗生素亲和力降低、PBPs增多或产生新的PBPs均可使抗生素失去抗菌作用。例如MRSA(methicillin resistant Staphylococcus aureus)具有多重耐药性,其产生机制是PBPs改变的结果,高度耐药性系由于原有的PBP2与PBP3之间产生一种新的PBP2'(即PBP2a),低、中度耐药系由于PBPs的产量增多或与甲氧西林等的亲和力下降所致;④细菌的细胞壁或外膜的通透性改变,使抗生素不能或很少进入细菌体内到达作用靶位。革兰阴性菌的外膜是限制β-内酰胺类抗生素透入菌体的第一道屏障。近年研究已证实抗生素透入外膜有非特异性通道与特异性通道两种。大肠杆菌K-12外膜有亲水性的非特异性孔道蛋白(porin)为三聚体结构,有二个孔道蛋白,即OmpF与OmpC,其合成由OmpB3基因调控。OmpF的直径为1nm,许多重要的β-内酰胺类抗生素大多经过此通道扩散入菌体内。鼠伤寒杆菌OmpF与OmpC缺陷突变株对头孢噻啶的通透性要比野生株小10倍,因而耐药。仅含微量OmpF与OmpC的大肠杆菌突变株,对头孢唑啉、头孢噻吩的透入也较野生株成倍降低,其MIC明显增高,也出现耐药。绿脓杆菌对β-内酰胺类抗生素耐药性的产生已证明是由于外膜非特异性孔道蛋白OPRF缺陷而引起的。革兰阴性外膜的特异性通道,在绿脓杆菌耐亚胺培南的突变株已证明系由于外膜缺失一种分子量为45~46kD蛋白OprD。如将此OprD重组于缺陷OprD的突变株外膜蛋白脂质体中,又可使亚胺培南透过性增加5倍以上,其MIC也相应地降低,于是细菌的耐药性消除。⑤由于细菌缺少自溶酶而出现细菌对抗生素的耐药性,即抗生素具有正常的抑菌作用,但杀菌作用差。
(一)青霉素
青霉素(penicillin G)又名苄青霉素(benzyl penicillin),是天然青霉素,侧链为苄基。常用其钠盐或钾盐,其晶粉在室温中稳定,易溶于水,水溶液在室温中不稳定,20℃放置24小时,抗菌活性迅速下降,且可生成有抗原性的降解产物,故青霉素应在临用前配成水溶液。
【抗菌作用】青霉素主要作用于革兰阳性菌、革兰阴性球菌、嗜血杆菌属以及各种致病螺旋体等。青霉素对溶血性链球菌、草绿色链球菌、肺炎球菌等作用强,肠球菌敏感性较差。不产生青霉素酶的金葡菌及多数表葡菌对青霉素敏感,但产生青霉素酶的金葡菌对之高度耐药。革兰阳性杆菌,白喉杆菌、炭疽杆菌及革兰阳性厌氧杆菌如产气荚膜杆菌、破伤风杆菌、难辨梭菌、丙酸杆菌、真杆菌、乳酸杆菌等皆对青霉素敏感。革兰阴性菌中脑膜炎球菌对青霉素高度敏感,耐药者罕见。对青霉素敏感的淋球菌日益少见。百日咳杆菌对青霉素敏感。致病螺旋体,如梅毒螺旋体、钩端螺旋体对之高度敏感。
【体内过程】青霉素遇酸易被分解,口服吸收差,肌注100万单位后吸收快且甚完全,0.5小时达血药浓度峰值,约为20U/ml,消除半衰期为1/2小时。6小时内静滴500万单位青霉素钠,2小时后能获得20~30U/ml的血药浓度。青霉素的血清蛋白结合率为46%~58%。青霉素主要分布于细胞外液,并能广泛分布于各种关节腔、浆膜腔、间质液、淋巴液、胎盘、肝、肾、肺、横纹肌、中耳液等。青霉素的脂溶性低,进入细胞量减少;房水与脑脊液含量也较低,但炎症时青霉素透入脑脊液和眼的量可略提高,能达有效浓度。青霉素几乎全部以原形迅速经尿排泄,约10%经肾小球过滤。90%经肾小管分泌。无尿患者青霉素t1/2可延长达10小时。丙磺舒可与青霉素竞争肾小管分泌,两药合用时能提高青霉素血药浓度,延长其半衰期。为了延长青霉素的作用时间,还可采用难溶制剂普鲁卡因青霉素和苄星青霉素;长效西林。它们的水悬剂或油制剂肌内注射后,在注射部位缓慢溶解吸收。普鲁卡因青霉素一次注射40万单位,可维持24小时,苄星青霉素溶解度极小,一次注射120万单位,可维持15天,这两种制剂的血药浓度很低,只用于轻症病人或用于预防感染。
【临床应用】青霉素为治疗A组和B组溶血性链球菌感染、敏感葡萄球菌感染、气性坏疽、梅毒、鼠咬热等的首选药。肺炎球菌感染和脑膜炎时也可采用,当病原菌比较耐药时,可改用万古霉素或利福平。青霉素也是治疗草绿色链球菌心内膜炎的首选药。还可作为放线菌病、钩端螺旋体病、梅毒、回归热等及预防感染性心内膜炎发生的首选药。破伤风、白喉病人采用青霉素时应与抗毒素合用。
【不良反应】青霉素的毒性很低,除其钾盐大量静注易引起高血钾症、肌内注射疼痛外,最常见的为过敏反应,有过敏休克、药疹、血清病型反应、溶血性贫血及粒细胞减少等。毒霉素制剂中的青霉噻唑蛋白、青霉烯酸等降解物、青霉素或6-APA高分子聚合物均可成为致敏原。为防止各种过敏反应,应详细询问病史,包括用药史,药物过敏史,家属过敏史,并进行青霉素皮肤过敏试验。应用青霉素及皮试时应作好急救准备,如肾上腺素、氢化可的松等药物和注射器材,以便一旦发生过敏休克,能及时治疗。
在青霉素治疗梅毒或钩端螺旋体病时可有症状加剧现象,称为赫氏反应(Herxheimerreaction),或治疗矛盾,此反应一般发生于青霉素开始治疗后6~8小时,于12~24小时消失,表现为全身不适、寒战、发热、咽痛、胁痛、心跳加快等;同时可有病变加重现象,甚至危及生命。此反应可能为螺旋体抗原与相应抗体形成免疫复合物的结果,或与螺旋体释放非内毒素致热原有关。
【用药注意】肌内注射局部可发生周围神经炎,鞘内注射和全身大剂量应用可引起青霉素脑痛。严重感染宜静脉滴注给药,大剂量静注应监测血清离子浓度,以防发生高血钠、高血钾症。
(二)半合成青霉素
1.耐酸青霉素 苯氧青霉素包括青霉素V和苯氧乙基青霉素。抗菌谱与青霉素相同,抗菌活性不及青霉素,耐酸、口服吸收好,但不耐酶,不宜用于严重感染。
2.耐酶青霉素 化学结构特点是通过酰基侧链(R1)的空间位障作用保护了β-内酰胺环,使其不易被酶水解,主要用于耐青霉素的金葡菌感染。
异恶唑类青霉素 侧链为苯基异恶唑,耐酸、耐酶、可口服。常用的有:苯唑西林、氯唑西林、双氯西林与氟氯西林。
【抗菌作用】本类药的抗菌谱及对耐药性金葡菌的作用均基本相似,对甲型链球菌和肺炎球菌效果最好,但不及青霉素,对耐药金葡菌的效力以双氯西林最强,随后依次为氟氯西林、氯唑西林与苯唑西林,对革兰阴性的肠道杆菌或肠球菌无明显作用。
【体内过程】胃肠道吸收较好,食物残渣会影响其吸收,因此,应在饭前一小时,空腹一次服药,大约1~1.5小时血药浓度达峰值,有效浓度可维持2~3小时。各药的吸收以苯唑西林最差,氯唑西林次之,双氯西林最好。血浆蛋白结合率均很高(95%以上)。主要以原型从尿排泄,速度较青霉素慢。
【临床应用】用于耐药金葡菌的各种感染,或需长期用药的慢性感染等。对严重金葡菌感染,宜注射给药。
3.广谱青霉素 对革兰阳性及阴性菌都有杀菌作用,还耐酸可口服,但不耐酶。
⑴氨苄西林(ampicillin) 对青霉素敏感的金葡菌等的效力不及青霉素,但对肠球菌作用优于青霉素。对革兰阴性菌有较强的作用,与氯霉素,四环素等相似或略强,但不如庆大霉素与多粘菌素,对绿脓杆菌无效。
【体内过程】口服后2小时达血药浓度峰值,经肾排泄,丙磺舒可延缓其排泄。体液中可达有效抗菌浓度,脑膜炎时脑脊液浓度较高。
【临床应用】主要用于伤寒、副伤寒、革兰阴性杆菌败血症、肺部、尿路及胆道感染等,严重者应与氨基甙类抗生素合用。
【不良反应】有轻微胃肠反应。
⑵阿莫西林(amoxycillin) 为对位羟基氨苄西林,抗菌谱与抗菌活性与氨苄西林相似,但对肺炎双球菌与变形杆菌的杀菌作用比氨苄西林强。经胃肠道吸收良好,血中浓度约为口服同量氨苄西林的2.5倍。阿莫西林用于治疗下呼吸道感染(尤其是肺炎球菌所致)效果超过氨苄西林。
⑶匹氨西林(pivampicillin) 为氨苄西林的双酯,口服吸收比氨苄西林好,能迅速水解为氨苄西林而发挥抗菌作用。正常人口服250mg,其血、尿浓度较相当剂量的氨苄西林分别高3与2倍。
4.抗绿脓杆菌广谱青霉素
⑴羧苄西林(cARBenicillin) 其抗菌谱与氨苄西林相似。特点是对绿脓杆菌及变形杆菌作用较强。口服吸收差,需注射给药,肾功能损害时作用延长,主要用于绿脓杆菌及大肠杆菌所引起的各种感染。单用时细菌易产生耐药性,常与庆大霉素合用,但不能混合静脉注射。毒性低,偶也引起粒细胞缺乏及出血。
⑵磺苄西林(sulbenicillin) 抗菌谱和羧苄西林相似,抗菌活性较强。口服无效,胆汁中药物浓度为血药浓度的3倍,尿中浓度尤高,主要用于治疗泌尿生殖道及呼吸道感染。副作用为胃肠道反应,偶有皮疹、发热等。
⑶替卡西林(ticarcillin) 抗菌谱与羧苄西林相似,抗绿脓杆菌活性较其强2~4倍。对革兰阳性球菌活性不及青霉素,口服不吸收,肌内注射后0.5~1.0小时达血药浓度峰值。分布广泛,胆汁中药物浓度高,大部分经肾排泄,主要用于绿脓杆菌所致各种感染。
⑷呋苄西林(furbenicillin) 抗绿脓杆菌较羧苄西林强6~10倍,对金葡菌、链球菌、痢疾杆菌等也有强大抗菌作用。副作用同羧苄西林。
⑸阿洛西林(azlocillin) 抗菌谱和羧苄西林相似,抗菌活性与哌拉西林相近,强于羧苄西林。对多数肠杆菌科细菌和肠球菌以及绿脓杆菌均有较强作用。对耐羧苄西林和庆大霉素的绿脓杆菌也有较好作用。主要用于治疗绿脓杆菌、大肠杆菌及其他肠杆菌科细菌所致的感染。
⑹哌拉西林(piperacillin) 抗菌谱广与羧苄西林相似,而抗菌作用较强,对各种厌氧菌均有一定作用。与氨基甙类合用对绿脓杆菌和某些脆弱拟杆菌及肠杆菌科细菌有协同作用。除产青霉素酶的金葡菌外,对其他革兰阴性球菌和炭疽杆菌等均甚敏感。不良反应较少,可供肌注及静脉给药。目前在临床已广泛应用。
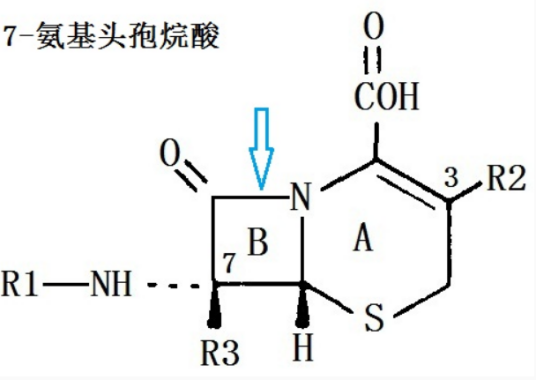
【化学与分类】头孢菌素类抗生素是从头孢菌素的母核7-氨基头孢烷酸(7-ACA)接上不同侧链而制成的半合成抗生素。本类抗生素具有抗菌谱广、杀菌力强、对胃酸及对β-内酰胺酶稳定,过敏反应少,(与青霉素仅有部分交叉过敏现象)等优点。根据其抗菌作用特点及临床应用不同,可分为三代头孢菌素。第一代头孢菌素的特点有:①对革兰阳性菌(包括对青霉素敏感或耐药的金葡菌)的抗菌作用较第二、三代强,对革兰氏阴性菌的作用较差;②对青霉素酶稳定,但仍可为革兰阴性菌的β-内酰胺酶所破坏;③对肾脏有一定毒性。
第二代头孢菌素的特点有:①对革兰阳性菌作用与第一代头孢菌素相仿或略差,对多数革兰阴性菌作用明显增强,部分对厌氧菌有高效,但对绿脓杆菌无效;②对多种β-内酰胺酶比较稳定;③对肾脏的毒性较第一代有所降低。
第三代头孢菌素的特点有:①对革兰阳性菌有相当抗菌活性,但不及第一、二代头孢菌素,对革兰阴性菌包括肠杆菌属和绿脓杆菌及厌氧菌如脆弱类杆菌均有较强的作用;②其血浆t1/2较长,体内分布广,组织穿透力强,有一定量渗入脑脊液中;③对β-内酰胺酶有较高稳定性;④对肾脏基本无毒性。
【抗菌作用及作用机制】抗菌谱广,多数革兰阳性菌对之敏感,但肠球菌常耐药;多数革兰阴性菌极敏感,除个别头孢菌素外,绿脓杆菌及厌氧菌常耐药。本类药与青霉素类,氨基甙类抗生素之间有协同抗菌作用。
头孢菌素类为杀菌药,抗菌作用机制与青霉素类相似,也能与细胞壁上的不同的青霉素结合蛋白(PBPs)结合(见图38-1,38-2)。
细菌对头孢菌素类与青霉素类之间有部分交叉耐药现象。
【体内过程】多需注射给药。但头孢氨苄、头孢羟氨苄和头孢克洛能耐酸,胃肠吸收好,可口服。头孢菌素吸收后,分布良好,能透入各种组织中,且易透过胎盘。在滑囊液、心包积液中均可获得高浓度。头孢呋辛和第三代头孢菌素多能分布于前列腺。第三代头孢菌素还可透入眼部眼房水。胆汁中浓度也较高。其中以头孢哌酮为最高,其次为头孢曲松。头孢呋辛、头孢曲松、头孢噻肟、头孢他定、头孢哌酮等可透过血脑屏障,并在脑脊液中达到有效浓度。多数头孢菌素的血浆t1/2均较短(0.5~2.0小时),但头孢曲松的t1/2最长,可达8小时。
【不良反应】常见者为过敏反应,偶可见过敏性休克,哮喘及速发型皮疹等,青霉素过敏者约有5%~10%对头孢菌素有交叉过敏反应;静脉给药可发生静脉炎;第一代的头孢噻吩、头孢噻啶和头孢氨苄大剂量时可出现肾脏毒性,这与近曲小管细胞损害有关。由于头孢菌素钠盐含钠量可达2.0~3.5Eq/g,大量静注时应注意高钠血症的发生。
头孢孟多、头孢哌酮等可出现双硫仑(disulfiram)样反应,第三代头孢菌素偶见二重感染或肠球菌、绿脓杆菌和念珠菌的增殖现象。头孢孟多、头孢哌酮高剂量可出现低凝血酶原血症。
【临床应用】
第一代头孢菌素,主要用于耐药金葡菌感染,常用头孢噻吩、头孢拉定、及头孢唑啉,后者肌注血浓度为头孢菌素类中最高,是一代中最广用的品种。口服头孢菌素主要用于轻、中度呼吸道和尿路感染。
第二代头孢菌素用以治疗大肠杆菌、克雷伯菌、肠杆菌、吲哚阳性变形杆菌等敏感菌所致的肺炎、胆道感染、菌血症、尿路感染和其他组织器官感染。应用较多的有头孢呋辛及头孢孟多等。
第三代头孢菌素治疗尿路感染以及危及生命的败血症、脑膜炎、肺炎等严重感染可获满意效果。第三代头孢菌素治疗脑膜炎球菌肺炎也可选用。头孢他定为目前临床应用的抗绿脓杆菌最强的抗生素,此外头孢哌酮也可选用。对肠杆菌科细菌头孢曲松和头孢噻肟相仿,头孢哌酮稍差。新生儿脑膜炎和肠杆菌科细菌所致的成人脑膜炎须选用第三代头孢菌素。
非典型β-内酰胺类抗生素
(一)头霉素类
头霉素(cephamycin)自链霉菌获得的β-内酰胺抗生素,有A、B、C三型,C型最强。抗菌谱广,对革兰阴性菌作用较强,对多种β-内酰胺酶稳定。头霉素化学结构与头孢菌素相仿,但其头孢烯母核的7位碳上有甲氧基。目前广泛应用者为头孢西丁(cefoxitin),抗菌谱与抗菌活性与第二代头孢菌素相同,对厌氧菌包括脆弱拟杆菌有良好作用,适用于盆腔感染、妇科感染及腹腔等需氧与厌氧菌混合感染。
(二)拉氧头孢
拉氧头孢(latamoxef)又名羟羧氧酰胺菌素(moxalactam),化学结构属氧头孢烯,1位硫为氧取代,7位碳上也有甲氧基,抗菌谱广,抗菌活性与头孢噻肟相仿,对革兰阳性和阴性菌及厌氧菌,尤其脆弱拟杆菌的作用强,对β-内酰胺酶极稳定,血药浓度维持较久。
(三)硫霉素类
硫霉素(thienamycin)化学结构属碳青霉烯类,噻唑环有饱和链,1位硫为碳取代,抗菌谱广,抗菌作用强,毒性低,但稳定性极差,无实用意义,亚胺培南(imipenem,亚胺硫霉素)具有高效、抗菌谱广、耐酶等特点。在体内易被去氢肽酶水解失活。所用者为本品与肽酶抑制剂西司他丁(cilaSTATin)的合剂,称为泰宁(tienam),稳定性好,供静脉滴注。
(四)β-内酰胺酶抑制剂
1.克拉维酸(clavulanic acid,棒酸) 为氧青霉烷类广谱β-内酰胺酶抑制剂,抗菌谱广,但抗菌活性低。与多种β-内酰胺类抗菌素合用时,抗菌作用明显增强。临床使用奥格门汀(augmentin,氨菌灵)与泰门汀(timentin),为克拉维酸分别和阿莫西林与替卡西林配伍的制剂。
2.舒巴坦(sulbactam,青霉烷砜) 为半合成β-内酰胺酶抑制剂,对金葡菌与革兰阴性杆菌产生的β-内酰胺酶有很强且不可逆抑制作用,抗菌作用略强于克拉维酸,但需要与其他β-内酰胺类抗生素合用,有明显抗菌协同作用。优立新(unasyn)为舒巴坦和氨苄西林(1:2)的混合物,可供肌肉或静脉注射。舒巴哌酮(sulperazone)为舒巴坦和头孢哌酮(1:1)混合物,可供在静脉滴注。
(五)单环β-内酰胺类抗生素
氨曲南(aztreonam)是第一个成功用于临床的单环β-内酰胺类抗生素,对需氧革兰阴性菌具有强大杀菌作用,并具有耐酶、低毒、对青霉素等无交叉过敏等优点,可用于青霉素过敏患者并常作为氨基甙类的替代品使用。