-
非诺贝特 编辑
中文名:非诺贝特
外文名:fenofibrate
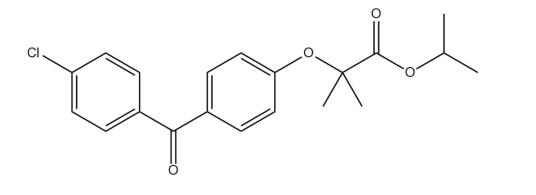
别名:普鲁脂芬、2-甲基-2-丙酸异丙酯
化学式:C20H21ClO4
CAS登录号:49562-28-9
熔点:80至81℃
沸点:469.8℃
水溶性:几乎不溶
密度:1.177g/cm³
外观:白色或淡黄色结晶性粉末
闪点:165.4℃
安全性描述:S36
危险性符号:Xn
危险性描述:R22
药品类型:化学药品
基本信息
化学式:C20H21ClO4
分子量:360.831
CAS号:49562-28-9
理化性质
密度:1.177 g/cm3
熔点:80-81ºC
沸点:469.8ºC
闪点:165.4ºC
折射率:1.547
外观:白色或淡黄色结晶粉末
分子结构数据
摩尔折射率:97.11
摩尔体积(cm3/mol):306.4
等张比容(90.2K):775.3
表面张力(dyne/cm):40.9
极化率(10-24cm3):38.49
计算化学数据
疏水参数计算参考值(XlogP):5.2
氢键供体数量:0
可旋转化学键数量:7
互变异构体数量:0
拓扑分子极性表面积:52.6
重原子数量:25
表面电荷:0
复杂度:458
同位素原子数量:0
确定原子立构中心数量:0
不确定原子立构中心数量:0
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:1
来源
本品为2-甲基-2-丙酸异丙酯,按干燥品计算,含C20H21ClO4不得少于98.5%。
性状
本品为白色或类白色结晶性粉末,无臭。
本品在三氯甲烷中极易溶解,在丙酮或乙醚中易溶,在乙醇中略溶,在水中几乎不溶。
熔点
本品的熔点(通则0612)应为78~82℃。
鉴别
1、取本品,加无水乙醇制成每1mL中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在286nm的波长处有最大吸收。
2、本品的红外光吸收图谱应与对照的图谱(光谱集248图)一致。
检查
乙醇溶液的澄清度与颜色
取本品1.0g,加乙醇25mL,振摇使溶解(必要时微温),溶液应澄清无色,如显色,与黄色1号标准比色液(通则0901第一法)比较,不得更深。
硫酸盐
取本品1.0g,加水50mL,振摇,在50℃加热10分钟,充分振摇使溶解,放冷,滤过,取滤液25mL,依法检查(通则0802),与标准硫酸钾溶液2.0mL制成的对照液比较,不得更浓(0.04%)。
氯化物
取本品1.0g,加水10mL,振摇,在50℃加热10分钟,充分振摇溶解,放冷,加水至20mL,滤过,取滤液10mL,依法检查(通则0801),与标准氯化钠溶液5.0mL制成的对照液比较,不得更浓(0.01%)。
照高效液相色谱法(通则0512)测定。
供试品溶液:取本品,加流动相溶解并稀释制成每1mL中约含0.4mg的溶液。
对照溶液:精密量取供试品溶液适量,用流动相定量稀释制成每1mL中含0.4µg的溶液。
系统适用性溶液:取杂质Ⅰ对照品与杂质Ⅱ对照品各适量,加流动相溶解并稀释制成每1mL中各含1µg的混合溶液。
色谱条件:用十八烷基硅烷键合硅胶为填充剂,以水(用磷酸调节pH值至2.5)-乙腈(30:70)为流动相,检测波长为286nm,进样体积10μL。
系统适用性要求:系统适用性溶液色谱图中,杂质Ⅰ峰与杂质Ⅱ峰之间的分离度应符合要求。
测定法:精密量取供试品溶液和对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度:供试品溶液的色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液的主峰面积(0.1%),各杂质峰面积的和不得大于对照溶液主峰面积的5倍(0.5%),小于对照溶液主峰面积0.1倍的色谱峰忽略不计。
残留溶剂
照残留溶剂测定法(通则0861第二法)测定。
内标溶液:取正丙醇,用N,N-二甲基甲酰胺稀释制成每1mL中约含1mg的溶液。
供试品溶液:取本品约1.0g,精密称定,置20mL顶空瓶中,精密加入内标溶液1mL与N,N-二甲基甲酰胺9mL,振摇使溶解,密封。
对照品溶液:分别取丙酮、异丙醇、三氯甲烷与甲苯各适量,精密称定,用N,N-二甲基甲酰胺定量稀释制成每1mL中分别约含1mg、1mg、0.012mg与0.178mg的混合溶液,精密量取5mL,置20mL顶空瓶中,精密加入内标溶液1mL与N,N-二甲基甲酰胺4mL,摇匀,密封。
色谱条件:以6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液,起始温度为40°C,维持8分钟,以每分钟45°C的速率升温至200°C,维持3分钟,进样口温度200℃,检测器温度250°C,顶空瓶平衡温度为80°C,平衡时间为30分钟。
系统适用性要求:对照品溶液色谱图中,各成分峰间的分离度均应符合要求。
测定法:取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度:按内标法以峰面积计算,丙酮、异丙醇、三氯甲烷与甲苯的残留量均应符合规定。
干燥失重
取本品,在50℃减压干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣
取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
含量测定
照高效液相色谱法(通则0512)测定。
供试品溶液
取本品约10mg,精密称定,置100mL量瓶中,加流动相适量,充分振摇使溶解,用流动相稀释至刻度,摇匀。
对照品溶液
取非诺贝特对照品约10mg,精密称定,置100mL量瓶中,加流动相适量,充分振摇使溶解,用流动相稀释至刻度,摇匀。
色谱条件
用十八烷基硅烷键合硅胶为填充剂,以水(用磷酸调节pH值至2.5)-乙腈(30:70)为流动相,检测波长为286nm,进样体积10µL。
系统适用性要求
理论板数按非诺贝特峰计算不低于3000。
测定法
精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
类别
降血脂药。
贮藏
遮光,密封保存。
制剂
1、非诺贝特片。
2、非诺贝特胶囊。
药理作用
非诺贝特为第三代苯氧乙乙酸类调血脂药物,药理作用类同于氯贝丁酯,但其降脂作用强,可以通过激活核受体,如过氧化物酶激活型增殖体受体(peroxisome proliferator~aCTivated receptor,PPAR),增加Apo AⅠ、Apo AⅡ及脂蛋白脂酶(LPL)的基因表达,减少Apo CⅢ的基因表达,从而增加血中Apo AⅠ、Apo AⅡ、HDL和LPL的浓度,降低血中appc Ⅲ的浓度,加速乳糜微粒及VLDL降解,降低TG和LDL水平,有利于防止动脉粥样硬化病变的发生与发展。长期应用毒性小,无蓄积作用,不与DNA结合,无致基因突变作用。
本品有显著降低血清甘油三酯和极低密度脂蛋白、胆固醇、低密度脂蛋白和载脂蛋白-B的浓度,并使高密脂蛋白、载脂蛋白-A1及载脂蛋白-A与载脂蛋白-B的比值升高,较氯贝丁酯作用为强。
药代动力学
口服后迅速吸收,体内分布符合二室模型,服药后4~7h血药浓度达峰值(20~30μg/mL),α相半衰期为4.9h,β相半衰期为26.6h。体内迅速被组织和血浆酶分解,形成与蛋白紧密结合的游离酸,仅10%为原形。80%所服剂量在94h内排出体外,6天内大于90%的代谢产物由尿排出,小部分随粪排出。
适应症
适用于除高脂蛋白血症II型和纯合子家族性高胆固醇血症外的各种高脂蛋白血症的治疗。最适用于治疗高三酰甘油血症及以TG增高为主的混合型高脂血症。
成人饮食控制疗法不理想的高胆固醇血症和/或高甘油三酯血症。
禁忌症
注意事项
长期服用者应定期进行肝肾功能检查,若有明显异常,应及时减量或停药。
1、本品毒性甚低,少数病人可见肝功能障碍、停药后2~4周恢复正常。
3、偶有口干、食欲不振、大便次数增多、皮疹、腹胀和白细胞减少等。
4、孕妇禁用;肝、肾功能不全者慎用。
孕妇及哺乳期妇女用药
孕妇及哺乳期妇女禁用。本品尚无用于人类的实验数据。
儿童用药
本品用于儿童的疗效和安全性,目前尚无实验研究加以证实,因此本品不能用于儿童。
老年用药
老年人单剂量口服本品的清除率与成年人相似,但如有肾功能不良时,须适当减少本品用药剂量。
不良反应
服药后偶有口干、食欲减退、大便次数增多、湿疹、失眠、乏力和性欲减退,停药后可消失。个别病例可见一过性转氨酶及尿毒氮或肌酐升高,一般停药后通迅速回到正常。
用法用量
每次0.1g,每天3次,饭后服用。微粒化非诺贝特(力平之200mg)吸收好,服用方便,常用剂量200mg,每晚1次。
1、微粒化胶囊:200mg qd,进餐时服用。标准化胶囊:100 mg tid或300 mg qd。维持剂量为100 mg bid或微粒化胶囊 200mg ,qd。
2、口服:每日300mg,可早餐后100mg,晚餐后200mg,或晚餐后300mg顿服。一般服药10日左右有明显疗效,2周左右(严重者4周左右)血脂恢复正常水平。此后,在饮食及运动配合下,维持量为每日100~200mg。儿童每公斤5mg。
药物相互作用
可能增强华法林等抗凝药的作用,同时服用抗凝药时,应检测凝血指标,注意调整剂量。
慎与其他降胆固醇药(其他贝特类,他汀类)同服。