-
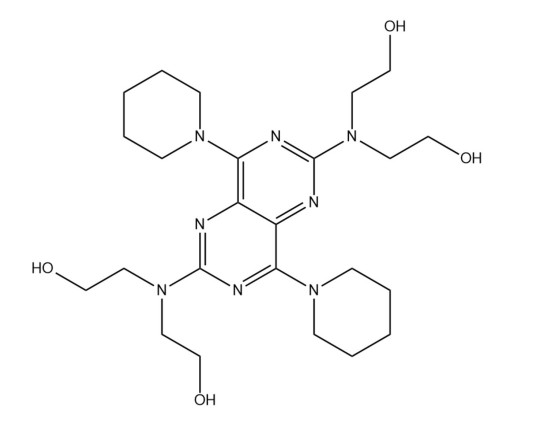
双嘧达莫 编辑
中文名:双嘧达莫
外文名:Dipyridamole
别名:潘生丁、2,6-双(二羟乙基氨基)-4,8-二哌啶基嘧啶并嘧啶
化学式:C24H40N8O4
分子量:504.626
CAS登录号:58-32-2
EINECS登录号:200-347-7
熔点:165至166℃
沸点:806.5℃
水溶性:微溶
密度:1.352g/cm³
外观:深黄色针状结晶
闪点:441.5℃
安全性描述:S26;S36
危险性符号:Xi
危险性描述:R36/37/38
基本信息
化学式:C24H40N8O4
分子量:504.626
CAS号:58-32-2
EINECS号:200-374-7
理化性质
密度:1.352 g/cm3
熔点:165-166ºC
沸点:806.5ºC
闪点:441.5ºC
折射率:1.666
外观:深黄色针状结晶
溶解性:易溶于甲醇、乙醇、氯仿,溶于pH3.3以下的稀酸,不太溶于丙酮、苯、乙酸乙酯,微溶于水
分子结构数据
摩尔折射率:139.39
摩尔体积(cm3/mol):373.0
等张比容(90.2K):1121.0
表面张力(dyne/cm):81.5
极化率(10-24cm3):55.2
疏水参数计算参考值(XlogP):0.7
氢键供体数量:4
可旋转化学键数量:12
互变异构体数量:0
拓扑分子极性表面积:145
重原子数量:36
表面电荷:0
复杂度:561
同位素原子数量:0
确定原子立构中心数量:0
不确定原子立构中心数量:0
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:1
用途
基本信息
本品为2,2',2'',2'''-嘧啶-2,6-二基)双次氮基]-四乙醇,按干燥品计算,含C24H40N8O4应为98.0%~102.0%。
性状
本品为黄色结晶性粉末,无臭。味微苦。
本品在三氯甲烷中易溶,在乙醇中溶解,在丙酮中微溶,在水中几乎不溶,在稀酸中易溶。
熔点
本品的熔点(通则0612)为162~168℃。
鉴别
1、取本品约10mg,加乙醇使溶解,即显绿色荧光,加酸后荧光消失。
2、取本品约10mg,加稀盐酸2mL使溶解,滴加1%铬酸钾溶液,即显红紫色,振摇后红紫色消褪,加过量1%铬酸钾溶液,红紫色不复现。
3、取本品,加0.01mol/L盐酸溶液制成每1mL中含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在283nm的波长处有最大吸收。
4、本品的红外光吸收图谱应与对照的图谱(光谱集557图)一致。
检查
含氯化合物
取本品约20mg,照氧瓶燃烧法(2010年版药典二部附录ⅦC)进行有机破坏,以0.4%氢氧化钠溶液20mL为吸收液,俟燃烧完毕后,强力振摇15分钟,加稀硝酸10mL,移至50mL纳氏比色管中,照氯化物检查法(2010年版药典二部附录ⅧA)检查,与对照液(与供试品同法操作,但燃烧时滤纸中不含供试品,并加标准氯化钠溶液4.0mL)比较,不得更浓(0.20%)。
照高效液相色谱法(通则0512)测定。
供试品溶液:取本品,加甲醇溶解并稀释制成每1mL中含1.0mg的溶液。
对照溶液:精密量取供试品溶液适量,用甲醇定量稀释制成每1mL中含10µg的溶液。
色谱条件:用十八烷基硅烷键合硅胶为填充剂,磷酸氢二钠溶液[取磷酸氢二钠0.25g,加水250mL溶解,用磷酸溶液(1→3)调节pH值至4.6] 甲醇(25:75)为流动相,检测波长为288nm,进样体积10µL。
系统适用性要求:理论板数按双嘧达莫峰计算不低于600。
测定法:精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度:供试品溶液色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液的主峰面积(1.0%)。
残留溶剂
照残留溶剂测定法(通则0861第二法)测定。
供试品溶液:取本品约0.1g,精密称定,置顶空瓶中,精密加入N,N-二甲基甲酰胺5mL使溶解,密封。
对照品溶液:分别取甲醇、丙酮与乙酸乙酯适量,精密称定,用N,N二甲基甲酰胺定显稀释制成每1mL中各约含50µg的溶液,精密植取5mL,置顶空瓶中,密封。
色谱条件:以6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液,起始温度为50℃,维持3分钟,以每分钟40°C的速率升温至160°C,维持3分钟,进样口温度为200℃,检测器温度为250°C,顶空瓶平衡温度为80℃,平衡时间为30分钟 。
系统适用性要求:对照品溶液色谱图中,各成分峰间的分离度均应符合要求。
测定法:取供试品溶液与对照品溶液,分别顶空进样,记录色谱图。
限度:按外标法以峰面积计算,甲醇、丙酮与乙酸乙酯的残留量均应符合规定。
干燥失重
取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣
取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
含量测定
取本品约0.3g,精密称定,加稀盐酸50mL溶解后,用溴酸钾滴定液(0.01667mol/L)缓缓滴定,临近终点时,时时振摇并逐滴加入,至不再出现红紫色即为终点。每1mL溴酸钾滴定液(0.01667mol/L)相当于25.23mg的C24H40N8O4。
类别
抗血小板聚集药、冠状动脉扩张药。
贮藏
遮光,密封保存。
制剂
1、双嘧达莫片。
2、双嘧达莫注射液。
3、双嘧达莫缓释胶囊。
药理毒理
具有抗血栓形成作用。双嘧达莫抑制血小板聚集,高浓度(50 μg/mL)可抑制血小板释放。
作用机制可能为:
3、抑制血栓烷素A2(TXA2)形成,TXA2血小板活性的强力激动剂;
4、增强内源性PGI2。
双嘧达莫对血管有扩张作用。犬经十二指肠给予双嘧达莫0.5~4.0 mg/kg产生剂量相关性体循环和冠状血管阻力降低,体循环血压降低和冠脉血流增加。给药后24分钟起效,作用持续约3小时。在人观察到相同的血流动力学效应。但急性静脉给药可使狭窄冠脉远端局部心肌灌注减少。在小鼠111周和大鼠128~142周口服试验中,8、25和75 mg/kg(1、3.1和 9.4倍于人每日最大推荐剂量)双嘧达莫未产生明显致癌效应。致突变试验的结果为阴性。大鼠生殖试验使用60倍于人每日最大推荐剂量双嘧达莫,未显示生殖受损的证据。但在115倍于人每日最大推荐剂量时,黄体数量明显减少,活胎种植减少。小鼠、大鼠和兔试验未显示双嘧达莫损害胎儿的证据。小鼠口服LD50为2150 mg/kg;单次口服致死量在大鼠为6000 mg/kg,在犬为 350 mg/kg。
药代动力学
双嘧达莫注射液:血浆半衰期为2~3小时。与血浆蛋白结合率高。在肝内代谢,与葡萄糖醛酸结合,从胆汁排泌。
双嘧达莫缓释胶囊:口服后血浆浓度达峰时间约2小时,血浆稳态峰浓度为1.98 μg/ml(1.01~3.99 μg/mL),稳态谷浓度为0.53 μg/mL(0.18~1.01 μg/mL)与血浆蛋白结合率为99%,半衰期约为12小时。在肝内代谢,与葡萄糖苷酸结合后从胆汁排泌。
用法用量
双嘧达莫注射液:0.142mg/(kg·min),静滴共4分钟。
双嘧达莫缓释胶囊:口服一次200mg,一日2次。
双嘧达莫片:口服。一次25~50mg,一日3次,饭前服。或遵医嘱。
注意事项
2、不宜与葡萄糖以外的其他药物混合注射。
3、与肝素合用可引起出血倾向。
4、有出血倾向患者慎用。
孕妇及哺乳期妇女用药
未在孕妇中作适当的对照研究,仅当确有必要方可用于孕妇。双嘧达莫从人乳汁中排泌,故哺乳期妇女应慎用。
儿童用药
12岁以下儿童用药的安全性和效果未确定。
药物相互作用
2、本品与双香豆素抗凝药同用时出血并不增多或增剧。
药物过量
如果发生低血压,必要时可用升压药。急性中毒症状在啮齿动物有共济失调、运动减少和腹泻,在狗中有呕吐、共济失调和抑郁。双嘧达莫与血浆蛋白高度结合,透析可能无益。
不良反应
有胃肠道反应、头痛、眩晕、疲劳、皮疹、潮红;静注时应缓慢,否则可引起低血压,特别是高血压病人;长期大量应用可致出血倾向。低血压病人慎用,心梗的低血压病人禁用。使用本品治疗缺血性心肌病,可能发生“冠状动脉窃血”,导致症状加重。