-
乙醇 编辑
中文名:乙醇
外文名:EthylAlcohol
别名:酒精、火酒
化学式:C2H5OH4
CAS登录号:64-17-5
EINECS登录号:200-578-6
熔点:-114.1℃(常压)
沸点:78.3℃(常压)
密度:0.7893g/cm³(20℃)
外观:无色透明液体,有芳香气味
闪点:14.0℃(闭杯);21.1(开杯)
应用:化学工业、医疗卫生、食品工业、农业生产等
安全性描述:S7;S16;S24/25;S26;S36/37;S45;S61
危险性符号:F
危险性描述:R11
UN危险货物编号:1170
CN危险货物编号:32061
危险标记:7(易燃液体)
爆炸极限:3.3%~19%
蒸气压:5.333kPa(19℃)
解离系数:pKa=15.9(25℃)
粘度:1.074mPa·s(20℃)
气体密度:2.009kg/m³
临界温度:516.2K
临界压力:6.38MPa
相对蒸气密度:1.59(空气=1)
同分异构体:二甲醚
折射率:1.3611(20℃)
溶解性:与水混溶,可混溶于乙醚、氯仿、甘油、甲醇等多数有机溶剂
相对密度:不大于0.8129;相当于含酒精不少于95.0%(ml/ml)
酒是古老的人造饮料,经考古发现,早在原始社会时期,人类就知道用谷物、瓜果发酵酿酒。中国是世界上最早酿酒的国家之一,甲骨文中就已经出现了“酒”字和与酒有关的“醴”“尊”“酉”等字。中国最晚在夏代已能人工造酒,《战国策》中记载“帝女令仪狄造酒,进之于禹”。殷商时期,中国已摆脱原始酿酒的方法,开始进入制曲酿酒阶段。周代酿酒已发展成独立且具有相当规模的手工业作坊。最初的酒是果酒和米酒。夏之后,经商周、历秦汉,以至于唐宋,都是以果实或粮食蒸煮,加曲发酵,经压榨、过滤后制得的酒。随着人类的进步发展,酿酒工艺也在原来基础上进一步发展,通过蒸馏提高了酒精的浓度,出现蒸馏酒。中国古人已发现酒在药用方面的价值,《汉书·食货志》中说:“酒,百药之长。”《本草纲目》认为:“酒少饮则和血行气,痛饮则伤神耗血,损胃之精,生痰动火。”
西方的酒品主要是谷物酒,长期沿用麦芽糖化加酵母的酿造法。直到19世纪90年代,法国人卡尔迈特从中国引进酒曲,从中分离出糖化力强并能起糖化作用的霉菌菌株,应用于酒精生产上,才突破了西方以麦芽糖化剂酿酒的传统工艺。关于酒的药用,19世纪医学家用白兰地治疗心衰和伤寒等症,生理学家和药理学家开始对酒精的药理作用进行研究,发现酒精能影响鸟的中枢神经活动,抑制蛙和哺乳动物的心跳,影响狗的胃肠消化吸收功能。
人们对酒含有的主要成分——乙醇的认识也在逐步发展。1784年,法国化学家安托万-洛朗·拉瓦锡(AntoineLaurent Lavoisier,1743—1794)首先测定了乙醇的元素成分。1807年,瑞士化学家尼古拉斯·泰奥多尔·索绪尔(Nicolas Theodore de Saussure,1767—1845)首先完成了乙醇的元素组成分析,确定了乙醇的化学式。1858年,英国化学家斯科特·库珀(Archibald Scott Couper,1831—1892)提出了乙醇最初的结构式,即库珀图解式。1825年,英国化学家迈克尔·法拉第(Michael FaraDAy,1791—1867)首次以合成方式制备乙醇。
乙醇的工业化生产从19世纪末开始发展起来,到第二次世界大战期间发酵法生产乙醇达到了高峰。发酵法是经典的乙醇生产方法,在相当长的时期里是乙醇的主要来源。但是发酵法受到原料来源和成本高的限制,因此合成法逐渐兴起。间接水合法制乙醇早在1825年就有报道,但直到1930年才由美国联合碳化物公司实现工业化。由于间接水合法要消耗大量的浓硫酸,生产过程中的硫酸介质对设备有严重腐蚀而且产品分离提纯困难,自1932年起美国和前苏联同时开始了直接水合法的研究。1945年,美国壳牌化学公司把磷酸吸附在颗粒状硅藻土上,制备成固体催化剂,解决了直接水合法的催化剂问题。20世纪50年代末,原联邦德国维巴化学公司在壳牌法基础上改进了催化剂。到20世纪60年代,美国伊斯特曼-柯达公司又在水合工艺方面进行了改进。20世纪60年代后期,前苏联对水合催化剂进行了改进,最后确定为磷酸-硅藻土催化剂。乙醇的生产方法除发酵法和合成法外,合成气制乙醇技术和甲醇同系化法也在开发中。
乙醇分子的球棍模型
乙醇是带有一个羟基的饱和一元醇,可以看成是乙烷分子中的一个氢原子被羟基取代的产物,或者是水分子中的一个氢原子被乙基取代的产物。乙醇分子是由C、H、O三种原子构成的极性分子,其中C、O原子均以sp³杂化轨道成键。
乙醇是一种透明清澈的无色液体,具有特有的酒味和刺激性味道,在25℃时亨利系数=5*10-6 atm-cu m/mol,电离势为10.47eV,20℃时折射率为1.3611可与多种有机溶剂混溶,与水以任意比例互溶,水-乙醇共沸物中乙醇的含量为95%,一体积乙醇加一体积水只产生1.92体积混合物,但乙醇与汽油混合时溶液总体积会增大。

乙醇的物理性质主要与其低碳直链醇的性质有关。分子中的羟基可以形成氢键,因此乙醇具有潮解性,可以很快从空气中吸收水分。分子间氢键的存在也使得乙醇的沸点高于相对分子质量相近的烷烃。乙醇分子中羟基的极性使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等;但氯化钠和氯化钾微溶于乙醇。非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。乙醇还可与水、乙腈、苯、丁酮、丁醛、四氯化碳、氯仿、环己烷、1,2-二氯乙烷、乙酸乙酯、乙基丁基醚、己烷、乙酸异丙酯、异丙醚、乙酸甲酯、甲基环己烷、硝基甲烷、甲苯、三氯乙烯等形成二元共沸物,使得它们不能通过蒸馏的方法进行分离。
性质 | 数据 | 性质 | 数据 | 性质 | 数据 |
|---|---|---|---|---|---|
熔点(常压) | -114.1 ℃ | 黏度(30 ℃) | 0.5142 mPa·s | van der Waals面积 | 4.930×109 cm2·mol-1 |
沸点(常压) | 78.3 ℃ | 蒸发热(沸点) | 38.95 kJ/mol | van der Waals体积 | 31.940 cm3·mol-1 |
密度(20 ℃) | 0.7893 g/cm3 | 熔化热 | 104.7 kJ/kg | 气相标准燃烧热 | 1410.01 kJ·mol-1 |
饱和蒸气压(20 ℃) | 5.8 kPa | 生成热(液体) | -277.8 kJ/mol | 气相标准生成热 | -234.01 kJ·mol-1 |
燃烧热 | -1365.5 kJ/mol | 比热容(20 ℃,定压) | 2.42 kJ/(kg·K) | 气相标准熵 | 280.64 J·mol-1·K-1 |
临界温度 | 243.1 ℃ | 沸点上升常数 | 1.03~1.09 | 气相标准生成自由能 | -166.7 kJ·mol-1 |
临界压力 | 6383.48 kPa | 电导率 | 1.35×10-19 S/m | 气相标准热容 | 65.21 J·mol-1·K-1 |
辛醇/水分配系数 | 0.32 | 热导率(30 ℃) | 0.1800 W/(m·K) | 液相标准燃烧热 | -1367.54 kJ·mol-1 |
闪点(闭杯) | 14.0 ℃ | 体膨胀系数(20 ℃) | 0.00108 K-1 | 液相标准生成热 | -276.98 kJ·mol-1 |
闪点(开杯) | 21.1 ℃ | 临界密度 | 0.275 g/cm3 | 液相标准熵 | 161.04 J·mol-1·K-1 |
引燃温度 | 363 ℃ | 临界体积 | 168 cm3·mol-1 | 液相标准生成自由能 | -174.18 kJ·mol-1 |
爆炸上限 | 19.0% | 临界压缩因子 | 0.241 | 液相标准热容 | 112.6 J·mol-1·K-1 |
爆炸下限 | 3.3% | 偏心因子 | 0.637 | 折射率(20 ℃) | 1.3611 |
黏度(15 ℃) | 0.6405 mPa·s | Lennard-Jones参数(A) | 4.5564 | 电偶极矩(25 ℃) | 5.67×10-30 C·M |
黏度(20 ℃) | 0.5945 mPa·s | Lennard-Jones参数(K) | 424.51 | 磁化率(20 ℃) | 7.34×10-7 |
黏度(25 ℃) | 0.5525 mPa·s | 26.421 (J·cm-3)0.5 | 介电常数(20 ℃) | 25.7 |
乙醇的官能团为羟基(—OH),因此化学性质主要受羟基以及受他影响的相邻基团的影响,主要的反应形式是О—H键和C—О键的断裂。羟基的结构特征是氧的电负性很大,分子中的C—О键和O—H键都是极性键,因而乙醇分子中有2个反应中心。由于α-H和β-H受到C—О键极性的影响具有一定的活性,因此它们还能发生氧化反应和消除反应等。
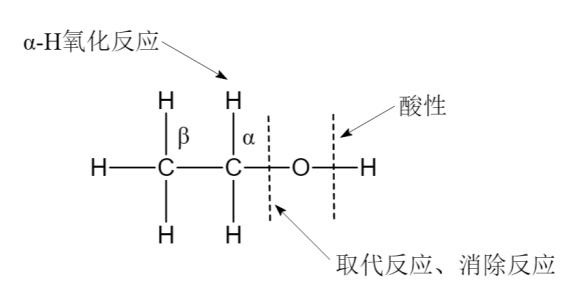 乙醇的化学性质与结构的关系
乙醇的化学性质与结构的关系
酸碱性
乙醇具有弱酸性(严格来说不具有酸性,因为不能使酸碱指示剂变色),因含有极化的氧氢键,故电离时会生成烷氧基负离子和质子。其电离方程式为:
乙醇的pKa=15.9(25 ℃),与水相近,电离平衡足以使乙醇与重水之间迅速发生同位素交换。其化学反应式为:
与金属反应
生成金属衍生物。乙醇与钠、钾等碱金属反应生成乙醇化物;低级醇容易发生此反应,有时有着火的危险。
高级醇反应较慢,特别是高级仲醇、叔醇反应速度小,不容易生成醇化物;铝、镁、钙、钡等金属与醇一起煮沸,也能生成醇化物。
酯化反应
生成酯醇。与有机酸、无机酸反应时脱水生成酯,反应是可逆的,反应方程式为:
乙醇也可与有机含氧酸脱水生成有机酸酯。以乙酸为例,在浓硫酸催化并加热的情况下,乙醇可与乙酸反应生成乙酸乙酯,其化学反应式为:
若是在化工产业中大规模的进行此反应,需设法生成物中移除水。酯类和酸或碱反应会产生醇类和盐,肥皂制作也是利用此反应的原理,因此称为皂化反应。
此反应常用强酸、金属盐、离子交换树脂等作催化剂;甲醇的反应性最大,C2~C5的伯醇反应速度大致相等;仲醇、叔醇的反应性小,而且叔醇在酸性介质中容易脱水生成烯烃,一般用间接的方法制备叔醇的酯;酰氯和酸酐与醇更易进行酯化反应。
卤化反应
乙醇可以和氢卤酸发生取代反应,生成卤代烃和水。其化学反应通式为:
反应活性顺序:HI>HBr>HCl。盐酸与乙醇的反应较困难,加无水氯化锌可催化反应的进行。无水氯化锌的浓盐酸溶液称为卢卡斯试剂(Lucas reagent)。乙醇可以溶解于卢卡斯试剂中,生成的氯乙烷则难溶,产生细小的油状液滴分散在卢卡斯试剂中,使反应液变浑浊。
乙醇也可与卤化磷(PX3、PX5)反应生成卤代烃,该方法更为常用。其化学反应通式为:
乙醇与PX5的反应,因副产物磷酸酯比较多,产物分离较为困难,因此不是制备卤代烃的好办法。实际工作中,三卤化磷常用卤素单质与磷的反应产生:
乙醇还可与氯化亚砜反应生成氯乙烷,其化学反应式为:
用氯化亚砜作为卤代试剂,副产物二氧化硫和氯化氢很容易离开反应体系,产物容易分离和纯化。
脱水反应
醇的脱水有分子间脱水和分子内脱水两种方式;分子间脱水生成醚(亲核取代反应),分子内脱水生成烯烃(消除反应)。
反应按哪种方式进行取决于醇的结构和反应条件;一般高温有利于生成烯烃,低温有利于生成醚;叔醇易脱水成烯,难以得到醚;反应常在催化剂存在下进行,常用的催化剂有硫酸、磷酸、三氧化二铝、磷酸铝等。
乙醇在催化剂存在的条件下加热,分子内消去一个水分子,生成乙烯。该反应属于消除反应,其化学反应式为:
乙醇发生分子间脱水生成乙醚的反应方程式为:
由于分子间脱水成醚的副反应较多,一般较少用于醚的合成。更加常用的是Williamson合成法,即用醇钠或酚钠与卤代烃反应,既可合成对称醚,也可合成不对称醚。以合成甲乙醚为例,其化学反应式为:
醇解反应
乙醇可与羧酸衍生物如酰卤、酸酐、酯等发生醇解反应生成相应的酯,难易程度不同。酰卤活性很高,醇解反应进行较快。以乙酰氯为例,其化学反应式为:
酸酐的醇解比酰卤缓和,反应中可用适量的酸或碱进行催化,是制备酯的常用方法。以乙酸酐为例,其化学反应式为:
酯的醇解反应可逆,需要在酸或碱的催化下进行,反应中从一个酯生成另一个新的酯,所以该反应也叫做酯交换反应。以乙酸甲酯为例,其化学反应式为:
氧化反应
乙醇的燃烧反应是广义上的氧化反应,乙醇在完全燃烧时会发出淡蓝色的火焰,生成二氧化碳和水,并放出大量的热,反应方程式为:
乙醇在不完全燃烧时生成一氧化碳,发出淡黄色火焰,放出大量热量,反应方程式为:
乙醇还可以发生脱氢反应,具体是伯醇或仲醇的蒸汽在高温下通过脱氢催化剂如铜、银、镍或铜、氧化铬时,则脱氢生成醛或酮。具体反应方程式为:
该反应可用于工业制乙醛。在人体内则可以通过乙醇脱氢酶(alcohol dehydrogenase,ADH)作用使乙醇变成乙醛。
叔醇不能脱氢,只能脱水成烯烃,伯醇氧化生成醛,醛再继续氧化成羧酸。仲醇氧化生成酮。叔醇难氧化,但在剧烈的条件下氧化生成碳原子数较叔醇少的产物。乙醇也可被高锰酸钾氧化成乙酸,同时高锰酸钾由紫红色变为无色。反应方程式为:
乙醇也可与酸化的三氧化铬溶液(或酸性重铬酸钾溶液)反应,当乙醇蒸汽进入含有酸化的三氧化铬(或酸性重铬酸钾溶液)的硅胶中时,可见硅胶由黄色变成草绿色,该反应可用于检验司机是否饮酒驾车。其化学反应式为:
强氧化剂如高锰酸钾及重铬酸钾都能将乙醇直接氧化成乙酸,反应不能停留在生成乙醛的阶段。使用特殊的氧化剂,如Sarrett试剂,可使反应停留在乙醛的阶段。Sarrett试剂是三氧化铬与吡啶形成的配合物,溶于盐酸后称为氯铬酸吡啶盐(Pyridinium chlorochromate,PCC)。反应一般在二氯甲烷中进行,反应方程式为:
乙醇氧化生成乙醛或乙酸。
卤仿反应
乙醛、甲基酮与次卤酸盐反应生成卤仿和少一个碳的羧酸盐的反应称为卤仿反应。由于乙醇在次卤酸盐条件下可氧化生成乙醛,故它也能发生卤仿反应。乙醇与次氯酸钠反应生成氯仿,溴仿和碘仿也可以分别由乙醇与次溴酸钠和次碘酸钠反应得到。在低碳醇中,只有乙醇才能进行卤仿反应。以乙醇与次碘酸钠反应为例,其过程如下:
其他
乙醇易与乙烯酮、环氧乙烷、异氰酸酯等反应性大的物质发生反应,分别生成乙酸酯、烷氧基醇和氨基甲酸乙酯;乙醇用漂白粉溶液氧化生成氯仿,用碘和氢氧化钾氧化生成碘仿;与不含亚硝酸的硝酸作用生成硝酸乙酯;与汞和过量的硝酸作用生成雷酸汞Hg(ONC)2;与氧化汞和氢氧化钠一起加热生成爆炸性物质C2Hg6O4H2。
1.按生产使用的原料可分为淀粉质原料发酵酒精、糖蜜原料发酵酒精、亚硫酸盐纸浆废液发酵生产酒精。
淀粉质原料发酵酒精(一般有薯类、谷类和野生植物等含淀粉质的原料,在微生物作用下将淀粉水解为葡萄糖,再进一步由酵母发酵生成酒精);
糖蜜原料发酵酒精(直接利用糖蜜中的糖分,经过稀释杀菌并添加部分营养盐,借酵母的作用发酵生成酒精);
亚硫酸盐纸浆废液发酵生产酒精(利用造纸废液中含有的六碳糖,在酵母作用下发酵成酒精,主要产品为工业用酒精。也有用木屑稀酸水解制作的酒精)。
2.按生产的方法来分,可分为发酵法、合成法两大类。
3.按产品质量或性质来分,又分为高纯度酒精、无水酒精、普通酒精和变性酒精。
4.按产品系列(BG384-81)分为优级、一级、二级、三级和四级。其中一、二级相当于高纯度酒精及普通精馏酒精。三级相当于医药酒精,四级相当于工业酒精。新增二级标准是为了满足不同用户和生产的需要,减少生产与使用上的浪费,促进提高产品质量而制订的。
1.发酵法:将富含淀粉的农产品如谷类、薯类等或野生植物果实经水洗、粉碎后,进行加压蒸煮,使淀粉糊化,再加入适量的水,冷却至60℃左右加入淀粉酶,使淀粉依次水解为麦芽糖和葡萄糖。然后加入酶母菌进行发酵制得乙醇。反应方程式为:

2.水合法:以乙烯和水为原料,通过加成反应制取。水合法分为间接水合法和直接水合法两种。
间接水合法也称硫酸酯法,反应分两步进行。先把95-98%的硫酸和50-60%的乙烯按2:1(重量比)在塔式反应器吸收反应,60-80℃、0.78-1.96MPa条件下生成硫酸酯。
第二步是将硫酸酯在水解塔中,于80-100℃、0.2-0.29MPa压力下水解而得乙醇,同时生成副产物乙醚。烯直接与水反应生成乙醇。反应方程式为:
直接水合法即一步法。由乙烯和水在磷酸催化剂存在下高温加压水合制得。本法流程简单、腐蚀性小,不需特殊钢材,副产乙醚量少,但要求乙烯纯度高,耗电量大。反应方程式为:

无论用发酵法或乙烯水合法,制得的乙醇通常都是乙醇和水的共沸物,即浓度为95%的工业乙醇。为获得无水乙醇,可用下列方法进一步脱水。(1)用生石灰处理工业乙醇,使水转变成氢氧化钙,然后蒸出乙醇,再用金属钠干燥;这是最老的方法。(2)共沸精馏脱水是目前工业上常用的方法。(3)用离子交换剂或分子筛脱水,然后再精馏。
3.在磷酸、硅藻土催化剂存在下,乙烯直接与水反应生成乙醇。
4.以工业乙醇为原料,经脱水处理,再在高效精馏塔内进行精馏,所得成品用微孔滤膜过滤即可。
5.选择含氧化钙高,铁、镁、硫杂质少的干燥生石灰,破碎成直径30mm的小块,并去除老灰、石头及消石灰,然后与2倍质量的工业乙醇混合,加热使乙醇回流,约18h后,脱水结束。快速蒸出乙醇,经精馏,去除少量头液,即可得99.5%以上的试剂无水乙醇。也可将95%的乙醇通过孔径4.2×10-9的Na型分子筛进行脱水和脱甲醇,然后再精馏。该分子筛可于400~500℃高温下烘3h,活化后,重新使用。
6.以乙二醇醋酸钾溶液为萃取剂,与工业乙醇等量混合后,在高效精馏塔中精馏,可获得99.7%以上的无水乙醇。
7.用戊烷或石油醚作为共沸剂于0.3~0.7MPa下精馏,可获得99.9%以上的无水乙醇。
8.在带有氯化钙干燥管的容器中加入制得的无水乙醇和适量金属钙,使金属钙充分吸收水分后,蒸馏可得符合气相色谱标准的无水乙醇,乙醇含量大于99.95%。也可以工业乙醇为原料,经恒沸精馏、气相制备色谱分离和纯化而得符合气相色谱标准的无水乙醇。
乙醇是重要的有机溶剂,广泛用于医药、涂料、卫生用品、化妆品、油脂等各个方法,占乙醇总耗量的50%左右。
乙醇是重要的基本化工原料,用于制造乙醛、乙二烯、乙胺、乙酸乙酯、乙酸、氯乙烷等等,并衍生出医药、染料、涂料、香料、合成橡胶、洗涤剂、农药等产品的许多中间体,其制品多达300种以上,但目前乙醇作为化工产品中间体的用途正在逐步下降,许多产品例如乙醛、乙酸、乙基乙醇已不再采用乙醇作原料而用其他原料代替。
消毒用品
不同浓度的消毒剂:
99.5%(体积分数)以上的酒精称为无水酒精。生物学中的用途:叶绿体中的色素能溶在有机溶剂无水乙醇(或丙酮)中,所以用无水乙醇可以提取叶绿体中的色素。
95%的酒精用于擦拭紫外线灯。这种酒精在医院常用,在家庭中则只会将其用于相机镜头的清洁。
70%~75%的酒精用于消毒。这是因为,过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死。若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也不能将细菌彻底杀死。其中75%的酒精消毒效果最好。
40%~50%的酒精可预防褥疮。长期卧床患者的背、腰、臀部因长期受压可引发褥疮,如按摩时将少许40%~50%的酒精倒入手中,均匀地按摩患者受压部位,就能达到促进局部血液循环,防止褥疮形成的目的。
25%~50%的酒精可用于物理退热。高烧患者可用其擦身,达到降温的目的。用酒精擦拭皮肤,能使患者的皮肤血管扩张,增加皮肤的散热能力,酒精蒸发,吸热,使病人体表面温度降低,症状缓解。
注意:酒精浓度不可过高,否则可能会刺激皮肤,并吸收表皮大量的水分。
饮料制品
乙醇是酒的主要成分,经过专门精制的乙醇也可用于制造其它饮料。乙醇还可用于制造醋酸、饮料、焙烤食品、糖果、冰淇淋、沙司等。
能源
与甲醇类似,乙醇可作能源使用。有的国家已开始单独用乙醇作汽车燃料或掺到汽油(10%以上)中使用以节约汽油。
有机溶剂
用作黏合剂、硝基喷漆、清漆、化妆品、油墨、脱漆剂等的溶剂以及制药工业中的分析试剂需要乙醇作为溶剂,还可用于溶解一些不溶于水的电镀有机添加剂。
有机原料
农药、医药、橡胶、塑料、人造纤维、洗涤剂、防冻液、燃料、消毒剂等的制造原料。在微电子工业中,用作脱水去污剂,可与去油剂配合使用。
1.疏水参数计算参考值(XlogP):-0.1
2.氢键供体数量:1
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:0
6.拓扑分子极性表面积:20.2 Ų
7.重原子数量:3
8.表面电荷:0
9.复杂度:2.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
环境危害
危险性:易挥发,易燃烧,刺激性。其蒸汽与空气混合成爆炸性气体。遇到高热、明火能燃烧或爆炸,与氧化剂铬酸、次氯酸钙、过氧化氢、硝酸、硝酸银、过氯酸盐等反应剧烈,有发生燃烧爆炸的危险。在火场中,受热的容器有爆炸危险。其蒸汽比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
防护措施
工程控制:密闭操作,加强通风。
呼吸系统防护:一般不需要特殊防护,高浓度接触时可佩带过滤式防毒面具(半面罩)。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防静电的胶布防毒衣。
手防护:戴一般作业防护手套(橡胶手套)。
其他防护:工作完毕,淋浴更衣。保持良好的卫生习惯。
不同暴露途径之急救方法
吸入:
将患者移离暴露区。如果呼吸停止,确实清通呼吸道并施行心肺复苏术。如果呼吸困难,给予氧气。保持患者温暖且休息。立即就医。
皮肤接触:以肥皂和水彻底清洗患部。立刻脱除污染的衣服。如果刺激性持绩,立即就医。
眼睛接触:立刻以大量水冲洗15分钟以上。眼皮应提离眼球以确保彻底清洗。立即就医。
食入:若患者意识清醒,给患者喝下1至3杯水或牛奶以稀释胃部内的含量。若患者自发性呕吐或催吐时,观察呼吸是否困难。不要对意识不清或半痉挛的患者催吐。保持患者温暖且休息。大量食入或有肠胃症状时,立即就医。
最重要症状及危害效应:刺激,吸入肺部可能引起肺炎。
对急救人员之防护:应穿着C级防护装备在安全区实施急救。
应急处置
迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。
小量泄漏:用砂土或其他不燃材料吸附或吸收。也可用大量水冲洗,洗水稀释后放入废水系统。
大量泄漏:构筑围堤或挖坑收容。用泡沫覆盖,降低蒸汽灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
乙醇的环境标准如下:
苏联 | 乙醇在生产区的临界量 | 2 t |
乙醇在贮存区的临界量 | 20 t | |
车间空气中有害物质的最高允许浓度 | 1000 mg/m3 | |
苏联(1977) | 大气质量标准 | 5.0 mg/m3 |
嗅觉阈浓度 | 50 mg/L |
吸入:可能刺激呼吸道和黏膜。可能引起危害中枢神经系统的作用,症状包括兴奋、陶醉、头痛、头昏眼花、困倦、视觉模糊、疲劳、战栗、痉挛、丧失意识、昏睡、呼吸停止和死亡。
皮肤:轻微刺激。
眼睛:暴露于液体、蒸汽、熏烟或雾滴可能引起中度刺激。直接接触可能引起刺激、痛、角膜可能会发炎甚至受到损害。
食入:1.可能引起危害中枢神经系统的作用,症状如“吸入”所列举。2.严重急性中毒可能引起血糖过低、体温过低和伸肌僵硬3吸入肺部可能引起肺炎。
LD50(测试动物、暴露途径) :7060 mg/kg(大鼠,吞食)
LC50(测试动物、暴露途径) :20,000 ppm/10H(大鼠,吞食)
局部效应:
20 mg/24H(兔子、皮肤)造成中等刺激
500 mg(兔子、眼睛)造成严重刺激
慢毒性或长期毒性:反复或长期接触皮肤可能导致脱脂、红、痒、发炎、龟裂及可能二度感染。长期皮肤接触,可能导致很少数人皮肤过敏反应。食入:慢性中毒可能引起肝脏、肾脏、大脑、肠胃道和心肌衰退。可能引起不良的繁殖影响。曾患肝病的人暴露其中可能增加危害性。与其他药物共同使用可能有不良作用。
特殊效应:200 mg/kg(性交前5天前的女人,子宫内)影响女生生殖力8 mg/kg(怀孕32周的女人,静脉注射)影响新生儿的Apgar计分值(乃新生儿心跳节律、呼吸、肌肉紧张度、反射刺激皮肤等综合推算值)。对水中生物具高毒性。
性状
本品为无色澄清液体,微有特臭,易挥发,易燃烧,燃烧时显淡蓝色火焰,加热至约78 ℃即沸腾。本品与水、甘油、三氯甲烷或乙醚能任意混溶。本品的相对密度(通则0601)不大于0.8129,相当于含C2H6O不少于95.0%(mL/mL)。
乙醇鉴别
1.取本品1 mL,加水5 mL与氢氧化钠试液1 mL后,缓缓滴加碘试液2 mL,即发生碘仿的臭气,并生成黄色沉淀。2.本品的红外光吸收图谱应与对照的图谱(光谱集1290图)一致。
乙醇检查
酸碱度取本品20 mL,加水20 mL,摇匀,滴加酚酞指示液2滴,溶液应为无色;再加0.01 mol/L氢氧化钠溶液1.0 mL,溶液应显粉红色。
溶液的澄清度与颜色
本品应澄清无色。取本品适量,与同体积的水混合后,溶液应澄清;在10 ℃放置30分钟,溶液仍应澄清。
吸光度
取本品,以水为空白,照紫外-可见分光光度法(通则0401)测定吸光度,在240 nm的波长处不得过0.08;250~260 nm的波长范围内不得过0.06;270~340 nm的波长范围内不得过0.02。
挥发性杂质
照气相色谱法测定法(通则0521)测定。
供试品溶液(1):取本品,即得。
供试品溶液(2):精密量取4-甲基-2-戊醇150 µL,置20 mL量瓶中,用本品稀释至刻度,摇匀,精密量取1 mL,置25 mL量瓶中,用本品稀释至刻度,摇匀。
对照溶液(1):精密量取无水甲醇100 µL,置50 mL量瓶中,用本品稀释至刻度,摇匀,精密量取5 mL,置50 mL量瓶中,用本品稀释至刻度,摇匀。
对照溶液(2):精密量取无水甲醇1 mL,乙醛1 mL,置10 mL量瓶中,用本品稀释至刻度,摇匀,精密量取100 μL,置10 mL量瓶中,用本品稀释至刻度,摇匀,再精密量取100 µL,置10 mL量瓶中,用本品稀释至刻度,摇匀。
对照溶液(3):精密量取乙缩醛150 µL,置50 mL量瓶中,用本品稀释至刻度,摇匀,精密量取100 µL,置10 mL量瓶中,用本品稀释至刻度,摇匀。
对照溶液(4):精密量取苯50 µL,置50 mL量瓶中,用本品稀释至刻度,摇匀,精密量取50 µL,置25 mL量瓶中,用本品稀释至刻度,摇匀。
色谱条件:以6%氰丙基苯基-94%二甲基聚硅氧烷为固定液(或极性相近);起始温度40 ℃,维持12分钟,以每分钟10 ℃的速率升温至240 ℃,维持10分钟;进样口温度为200 ℃,检测器温度为280 ℃,载气为氦气或氮气,进样体积1 µL。
系统适用性要求:对照溶液(2)色谱图中,乙醛峰与甲醇峰之间的分离度应符合要求。
测定法:取供试品溶液(1)(2)与对照溶液(1)(2)(3)(4),分别注入气相色谱仪,记录色谱图。
限度:供试品溶液(1)如出现杂质峰,甲醇峰面积不得大于对照溶液(1)中甲醇峰面积的0.5倍(0.02%);含乙醛和乙缩醛的总量按公式⑴计算,总量不得过0.001%(以乙醛计);含苯按公式(2)计算,不得过0.0002%;供试品溶液(2)中其他杂质峰面积的和不得大于4-甲基-2-戊醇的峰面积(0.03%,以4-甲基-2-戊醇计)。
乙醇和乙缩醛的总含量=+{×(Mr1/Mr2)}
式中,AE为供试品溶液(1)中乙醛的峰面积;AT为对照溶液(2)中乙醛的峰面积;CE为供试品溶液(1)中乙缩醛的峰面积;CT为对照溶液(3)中乙缩醛的峰面积;Mr1为乙醛的分子量,44.05;Mr2为乙缩醛的分子量,118.2。苯含量%=(0.0002%×BE)/(BT-BE),式中,BE为供试品溶液(1)中苯的峰面积;BT为对照溶液(4)中苯的峰面积。
不挥发物
取本品40 mL,置105 ℃恒重的蒸发皿中,于水浴上蒸干后,在105 ℃干燥2小时,遗留残渣不得过1 mg。
类别
消毒防腐药、溶剂。
贮藏
遮光,密封保存。
储存方法
储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。保持容器密封。应与氧化剂、酸类、碱金属、胺类等分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
运输信息
危险货物编号:32061
UN编号:1170
包装标志:7(易燃液体)
包装类别:O52
包装方法:
小开口钢桶;小开口铝桶;螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外木板箱。螺纹口玻璃瓶、塑料瓶或镀锡薄钢板桶(罐)外满底板花格箱、纤维板箱或胶合板箱。
运输注意事项:
铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。本品运输时限使用钢制企业自备罐车装运,运装前需报有关部门批准。运输时运输车辆应配备相应品种和数量的消防器材及泄漏应急处理设备。夏天最好早晚运输。运输时所使用的的槽(罐)车应有接地链,槽内可设孔隔板以减少震荡产生静电。应单独运输,严禁与酸类、易燃物、有机物、氧化剂、自燃物品、遇湿易燃物品等并车混运。运输途中应防暴晒、雨淋、防高温。中途停留时应远离火种、热源、高温区。装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。公路运输时要按照规定路线行驶,勿在居民区和人口稠密区停留。铁路运输时要禁止溜放。严禁用木船、水泥船散装运输。
密度瓶法
密度瓶法是一种较为经典的检测方法,使用的设备简单易于普及。其原理:以蒸馏法去除样品中的不挥发性物质,用密度瓶测定馏出液(酒精水溶液)20℃时的密度,根据馏出液的密度,求得20℃时乙醇的体积百分数,即酒精度。在啤酒、白酒、葡萄酒和果酒的国家标准分析方法中,密度瓶法均被列为乙醇测定的首选方法。该法精确度高,但需称重和蒸馏等繁琐操作,时间较长,而且对密度瓶的恒温要求极高,需严格控制温度在20∙0℃ ±0∙1℃
折光率法
每种纯液体在一定温度下都有固定的折光率,这是液体的特征常数之一。乙醇和甲醇的折光率差异明显。在20℃时,水的折光率为1.3330,随着水中乙醇浓度的增加,其折光率呈有规律的上升,其上升值与加入乙醇的量成正比;当甲醇存在时,折光率会随着甲醇浓度的增加而降低。因此,测定酒样的折光率就可以得知乙醇含量。
酒精计法
酒精计是基于阿基米德定律制成的一种测定酒精水溶液中乙醇的体积百分含量的专用仪器,测定时将其沉入样品中,直接读取酒精计的示值,同时测定温度,加以温度校正,求得20℃时乙醇的体积百分数。读数时,酒精计不可接触量筒壁,示值应以酒精计刻度与液体水平线形成的弯月面下缘为准。现行蒸馏酒与配制酒的国家标准分析方法中乙醇浓度采用酒精计法。该法操作简便快速,但准确度较差,受酒中其他非乙醇成分的影响大,只适用于乙醇的水溶液。
化学氧化法
化学氧化法的实质是碘量滴定法。其原理是在酸性溶液中,被蒸出的乙醇与过量重铬酸钾作用,乙醇被氧化为乙酸:剩余的重铬酸钾用碘化钾还原,析出的碘用硫代硫酸钠标准溶液滴定。根据硫代硫酸钠标准溶液的用量计算酒样中乙醇含量。该法与国标密度瓶法相比具有快速的特点,与酒精计法相比具有结果准确的优点。此法测定的乙醇浓度比较低,其下限可达0∙02%,故还可用于测定酒中低含量的乙醇。
分光光度法
分光光度法是以生成有色化合物的显色反应或褪色反应为基础,通过测量有色物质溶液吸光度来确定待测组分含量的方法。
荧光光度法
荧光光度法简单快速,灵敏度高,线性范围宽,选择性好。
气相色谱法
气相色谱(GC)法测定酒中乙醇含量,具有较高的灵敏度与特异性。其原理为试样被气化后,随同载气进入色谱柱,利用被测定的各组分在气液两相中具有不同的分配系数,在柱内形成迁移速度的差异而分离。分离后的组分先后流出色谱柱,进入氢火焰离子化检测器(FID)检测。根据色谱图上各组分色谱峰的保留时间与标样相对照进行定性;利用峰面积或峰高,用内标或外标法定量。
激光拉曼光谱法
激光拉曼光谱法作为一种新型无损检测技术,广泛应用于样品的定性、定量分析。其原理是利用乙醇激光拉曼光谱中-CCO面内伸缩振动峰为特征峰(884/cm),以本底水的拉曼特征峰(3200/cm)为内标,通过峰高比值法测定乙醇浓度的响应值。
近红外光谱法
近红外光是指介于可见光和中红外光之间的电磁波波长在750~2500nm(波数范围13330~4000/cm)之间,一般有机物在该谱区的近红外光谱吸收主要是含氢基团(C-H,O-H,N-H,S-H等)的倍频与合频的振动吸收。由于几乎所有的有机物的一些主要结构和组成都可以在他们的近红外光谱中找到信号,而且谱图稳定,获取光谱容易。因此近红外光谱法被誉为分析的巨人。但作为信息源的近红外光谱区的波频和吸收信号均较弱,谱带多且相互重叠,以致信息解析相当困难。随着计算机与化学计量学的深入研究和广泛应用,近红外光谱技术成为发展最快、最引人注目的光谱技术之一。
微生物电极法
微生物电极法的原理是从土壤中分离得到的一株好氧乙醇菌,该菌能很好的降解乙醇。用PVC、纤维素等材料将其包埋,制备的微生物膜与极谱型氧电极结合,制成乙醇微生物电极,在pH 6∙4~7∙3的磷酸盐缓冲液中,温度34℃ ±0∙5℃,以0∙6L/min的流量连续向溶液中鼓入空气。电极空白电流I0稳定后,加入乙醇标准溶液。乙醇分子扩散进入微生物膜被膜内微生物同化而耗氧,致使电极输出电流下降并迅速达到新的稳态值It,电流降低值ΔI(ΔI= I0-It)在一定浓度范围内与乙醇浓度呈线性关系。
(1)乙醛:乙醇氧化或气相脱氢生产乙醛曾是工业乙醇的主要用途。乙醛在工业上大量用于合成乙酸、丁醇、季戊四醇等有机产品,也用于生产聚乙醛、三氯乙醛等产品。
(2)乙胺:乙胺是由乙醇与氨经催化反应生成的,同时得到乙胺、二乙胺和三乙胺。乙胺、二乙胺可作溶剂,也可用来制造洗涤剂、润滑剂和橡胶促进剂、农药、染料、医药以及抗氧剂等。三乙胺除用作有机溶剂外,在合成树脂中可用作聚碳酸酯光气法的催化剂和四氟乙烯的阻聚剂,也可用作食品防腐剂、农药和染料生产的原料,国防工业上可用作高能燃料。
(3)乙酸乙酯:由乙酸和乙醇酯化得到,是纤维素酯的低沸点溶剂,可用作人造革、火药、食品工业中的食用香精、纤维照像膜片及医药和染料等方面的原料。










