-
比热容 编辑
中文名:比热容
外文名:specificheatcapacity
所属学科:热力学
别名:比热容量
简称:比热
符号:c
计算式:c=Q/m(t-t0)
国际(SI)单位:焦耳每千克开尔文
常用单位:焦耳每千克摄氏度
水的比热容较大,在工农业生产和日常生活中有广泛的应用。这个应用主要考虑两个方面,第一是一定质量的水吸收(或放出)很多的热而自身的温度却变化不大,有利于调节气候;第二是一定质量的水升高(或降低)一定温度吸热(或放热)很多,有利于用水作冷却剂或取暖。
调节气候
水的比热容较大,对于气候的变化有显著的影响。在同样受热或冷却的情况下,水的温度变化较小,水的这个特征对气候影响很大,白天沿海地区比内陆地区升温慢,夜晚沿海温度降低少,为此一天中沿海地区温度变化小,内陆温度变化大,一年之中夏季内陆比沿海炎热,冬季内陆比沿海寒冷。当环境温度变化较快的时候,水的温度变化相对较慢。生物体内水的比例很高,有助于调节生物体自身的温度,以免温度变化太快对生物体造成严重损害。海陆风的形成原因与之类似。
1.对气温的影响
据新华社消息,三峡水库蓄水后,这个世界上最大的人工湖将成为一个天然“空调”,使山城重庆的气候冬暖夏凉。据估计,夏天气温可能会因此下降5℃,冬天气温可能会上升3到4℃。
2.热岛效应的缓解
晴朗无风的夏日,海岛上的地面气温,高于周围海上气温,并因此形成海风环流以及海岛上空的积云对流,这是海洋热岛效应的表现。水的比热容是沙石的4倍多。质量相同的水和沙石,要使它们上升同样的温度,水会吸收更多的热量;如果吸收或放出的热量相同,水的温度变化比沙石小得多。夏天,阳光照在海上,尽管海水吸收了许多热量,但是由于它的比热容较大,所以海水的温度变化并不大,海边的气温变化也不会很大。而在沙漠,由于沙石的比热容较小,吸收同样的热量,温度会上升很多,所以沙漠的昼夜温差很大。海岸昼夜温差变化比沙漠中小,适于居住。2010~2013年以来,由于城市人口集中,工业发达,交通拥塞,大气污染严重,且城市中的建筑大多为石头和混凝土建成,在温度的空间分布上, 城市犹如一个温暖的岛屿,从而形成城市热岛效应。在缓解热岛效应方面,专家测算,一个中型城市环城绿化带树苗长成浓荫后,绿化带常年涵养水源相当于一座容积为1.14×10m3的中型水库,由于水的比热容大,能使城区夏季高温下降1℃以上,有效缓解日益严重的“热岛效应”。
水库的建立,水的增加,而水的比热容大,在同样受冷受热时温度变化较小,从而使夏天的温度不会升得比过去高,冬天的温度不会下降得比过去低,使温度保持相对稳定,从而水库成为一个巨大的“天然空调”。
运用领域
1.水冷系统的应用
人们很早就开始用水来冷却发热的机器,在电脑CPU散热中可以利用散热片与CPU核心接触,使CPU产生的热量通过热传导的方式传输到散热片上,然后利用风扇将散发到空气中的热量带走。但水的比热容远远大于空气,因此可以用水代替空气作为散热介质,通过水泵将内能增加的水带走,组成水冷系统。这样CPU产生的热量传输到水中后水的温度不会明显上升,散热性能优于上述直接利用空气和风扇的系统。
武器:第一次世界大战和第二次世界大战当中,一些武器使用的是水冷式枪管;一些战斗机和轰炸机的引擎使用的是水冷式引擎。
热机(例如汽车的发动机,发电厂的发电机等)的冷却系统也用和水做为冷却液,也是利用了水的比热容大这一特性。
2.农业生产上的应用
水稻是喜温作物,在每年三四月份育苗的时候,为了防止霜冻,农民普遍采用“浅水勤灌”的方法,即傍晚在秧田里灌一些水过夜,第二天太阳升起的时候,再把秧田中的水放掉。根据水的比热容大的特性,在夜晚降温时,使秧苗的温度变化不大,对秧苗起了保温作用。
3.热水取暖
冬季供热用的散热器、暖水袋。我国北方楼房中的“暖气”用水作为介质,把燃料燃烧时产生的热量带到房屋中取暖。
4.其他
诸如在炎热的夏天古代皇室用流水从屋顶上流下,起了防暑降温作用。
其它信息参见词条定压比热容、定容比热容。
比热容是热力学中常用的一个物理量,表示物质提高温度所需热量的能力,而不是吸收或者散热能力。它指单位质量的某种物质升高(或下降)单位温度所吸收(或放出)的热量。其国际单位制中的单位是焦耳每千克开尔文,即令1kg的物质的温度上升1开尔文所需的热量。根据此定理,最基本便可得出以下公式:
物质的比热容越大,相同质量和温升时,需要更多热能。以水和油为例,水和油的比热容分别约为4200 Jkg-1K-1和2000 Jkg-1K-1,即把相同质量的水加热的热能比油多出约一倍。若以相同的热能分别把相同质量的水和油加热的话,油的温升将比水的温升大。
卡诺定理指出,可逆循环的效率只与高温热源和低温热源的温度有关,而与工作物质(工质)或工作路径等其它因素无关。
热力学温度又被称为绝对温度,是热力学和统计物理中的重要参数之一。一般所说的绝对零度便是对应-273.15摄氏度。
一定质量的物质,在温度升高时,所吸收的热量与该物质的质量和升高的温度乘积之比,称作这种物质的比热容(比热),用符号c表示。其国际单位制中的单位是焦耳每千克开尔文,其常用单位之一是焦耳每千克摄氏度。J是指焦耳,K是指热力学温标,即令1千克的物质的温度上升(或下降)1开尔文所需的能量。根据此定理,便可得出以下公式:
Q为吸收(或放出)的热量;m是物体的质量,ΔT是吸热(或放热)后温度的变化量,初中的教材里把ΔT写成Δt,其实这是不规范的(我们生活中常用℃作为温度的单位,很少用K,而且ΔT=Δt,因此中学阶段都用Δt,但国际或更高等的科学领域仍用ΔT)。
物质的比热容与所进行的过程有关。在工程应用上常用的有定压比热容Cp、定容比热容Cv和饱和状态比热容三种。
定压比热容Cp:是单位质量的物质在压力不变的条件下,温度升高或下降1℃或1K所吸收或放出的能量。
定容比热容Cv:是单位质量的物质在容积(体积)不变的条件下,温度升高或下降1℃或1K吸收或放出的能量。
饱和状态比热容:是单位质量的物质在某饱和状态时,温度升高或下降1℃或1K所吸收或放出的热量。
比热容的单位是复合单位。
在国际单位制中,能量、功、热量的主单位统一为焦耳,温度的主单位是开尔文,因此比热容的国际单位为J·kg-1 ·K-1,读作“焦(耳)每千克开(尔文)”。
常用单位:J/(kg·℃)、J/(g·℃)、kJ/(kg·℃)、cal/(kg·℃)、kcal/(kg·℃)等。注意摄氏度和开尔文仅在温标表示上有所区别,在表示温差的量值意义上等价,因此这些单位中的℃和K可以任意互相替换。例如“焦每千克摄氏度”和“焦每千克开”是等价的。
设有一质量为m的物体,在某一过程中吸收(或放出)热量ΔQ时,温度升高(或降低)ΔT,则ΔQ/ΔT称为物体在此过程中的热容量(简称热容),用C表示,即
一般情况下,热容与比热容均为温度的函数,但在温度变化范围不太大时,可近似地看为常量。于是有
如令温度改变量
则有:
这是中学中用比热容来计算热量的基本公式。
在英文中,比热容被称为:Specific Heat Capacity(Shc)。
用比热容计算热能的公式为:能量=质量×比热×温度变化
可简写为:Energy=SHC×Mass×Temp Ch,
与比热相关的热量计算公式:Q=cmΔT,即Q吸(放)=cm(T初-T末),其中c为比热,m为质量,Q为能量热量。吸热时为Q=cmΔT升(用实际升高温度减物体初温),放热时为Q=cmΔT降(用实际初温减降后温度)。或者Q=cmΔT=cm(T末-T初),Q>0时为吸热,Q<0时为放热。
比热容的计算公式一般为
c表示比热容
m表示物体的质量
to表示物体的初温
t表示物体的末温
(△t:物体变化温度,即t-t0)
这是用来计算物体温度升高时的公式。若物体降低时,则是用物体的初温度减去末温度。
比热容的计算公式也写作
在实验过程中,液态水的定压比热容经常会被用来计算吸收或放出的热量,水作为最常见的物质,它的比热数据较易获得,当实验要求精度不高时,可近似认为常压下水的定压比热为4.2kJ/(kg·℃)。
下面给出在不同压力,不同温度下的液态水的定压比热容Cp的数据(单位:kJ/(kg·℃))
压力 x10^5 Pa | 温度(摄氏度) | ||||||||
0 | 20 | 50 | 100 | 150 | 200 | 250 | 300 | 350 | |
1 | 4.217 | 4.182 | 4.181 | ||||||
5 | 4.215 | 4.181 | 4.180 | 4.215 | 4.310 | ||||
10 | 4.212 | 4.179 | 4.179 | 4.214 | 4.308 | ||||
50 | 4.191 | 4.166 | 4.170 | 4.205 | 4.296 | 4.477 | 4.855 | 3.299 | |
100 | 4.165 | 4.151 | 4.158 | 4.194 | 4.281 | 4.450 | 4.791 | 5.703 | 4.042 |
150 | 4.141 | 4.137 | 4.148 | 4.183 | 4.251 | 4.425 | 4.735 | 5.495 | 8.863 |
200 | 4.117 | 4.123 | 4.137 | 4.173 | 4.252 | 4.402 | 4.685 | 5.332 | 8.103 |
250 | 4.095 | 4.109 | 4.127 | 4.163 | 4.239 | 4.379 | 4.639 | 5.201 | 7.017 |
300 | 4.073 | 4.097 | 4.117 | 4.153 | 4.226 | 4.358 | 4.598 | 5.091 | 6.451 |
单位质量的某种物质,温度降低1度放出的热量,与它温度升高一度吸收的热量相等,数值上也等于它的比热容。
 比热容
比热容
物质 | 化学符号 | 模型 | 状态 | 比热容量(基本) J/(kg·℃) | 比热容量(25℃)J/(kg·K) |
|---|---|---|---|---|---|
H | 2 | 气 | 14000 | 14300 | |
氦 | He | 1 | 气 | 5190 | 5193.2 |
氨 | NH3 | 4 | 气 | 2055 | 2050 |
氖 | Ne | 1 | 气 | 1030 | 1030.1 |
锂 | Li | 1 | 固 | 3580 | 3582 |
C2H5OH | 9 | 液 | 2460 | 2440 | |
汽油 | 混 | 混 | 液 | 2200 | 2220 |
CnH2n+2 | 62至122 | 固 | 2200 | 2500 | |
CH4 | 5 | 气 | 2160 | 2156 | |
油 | 混 | 混 | 液 | 2000 | 2000 |
软木塞 | 混 | 混 | 固 | 2000 | 2000 |
C2H6 | 8 | 气 | 1730 | 1729 | |
尼龙 | 混 | 混 | 固 | 1700 | 1720 |
乙炔 | C2H2 | 4 | 气 | 1500 | 1511 |
CH2 | 3 | 固 | 1300 | 1300 | |
硫化氢 | H2S | 3 | 气 | 1100 | 1105 |
N | 2 | 气 | 1040 | 1042 | |
空气(室温) | 混 | 混 | 气 | 1030 | 1012 |
空气(海平面、干燥、0℃) | 混 | 混 | 气 | 1005 | 1035 |
O | 2 | 气 | 920 | 918 | |
CO2 | 3 | 气 | 840 | 839 | |
一氧化碳 | CO | 2 | 气 | 1040 | 1042 |
铝 | Al | 1 | 固 | 900 | 897 |
石绵 | 混 | 混 | 固 | 840 | 847 |
陶瓷 | 混 | 混 | 固 | 840 | 837 |
氟 | F | 2 | 气 | 820 | 823.9 |
砖 | 混 | 混 | 固 | 750 | 750 |
石墨 | C | 1 | 固 | 720 | 710 |
四氟甲烷 | CF4 | 5 | 气 | 660 | 659.1 |
SO2 | 3 | 气 | 600 | 620 | |
玻璃 | 混 | 混 | 固 | 600 | 840 |
氯 | Cl2 | 2 | 气 | 520 | 520 |
钻石 | C | 1 | 固 | 502 | 509.1 |
钢 | 混 | 混 | 固 | 460 | 450 |
Fe | 1 | 固 | 460 | 444 | |
黄铜 | Cu,Zn | 混 | 固 | 380 | 377 |
铜 | Cu | 1 | 固 | 385 | 386 |
银 | Ag | 1 | 固 | 235 | 233 |
汞 | Hg | 1 | 液 | 139 | 140 |
铂 | Pt | 1 | 固 | 135 | 135 |
金 | Au | 1 | 固 | 129 | 126 |
铅 | Pb | 1 | 固 | 125 | 128 |
水蒸气(水) | H2O | 3 | 气 | 1850 | 1850 |
水 | H2O | 3 | 液 | 4200 | 4186 |
冰(固态水) | H2O | 3 | 固 | 2100 | 2050 (-10℃) |
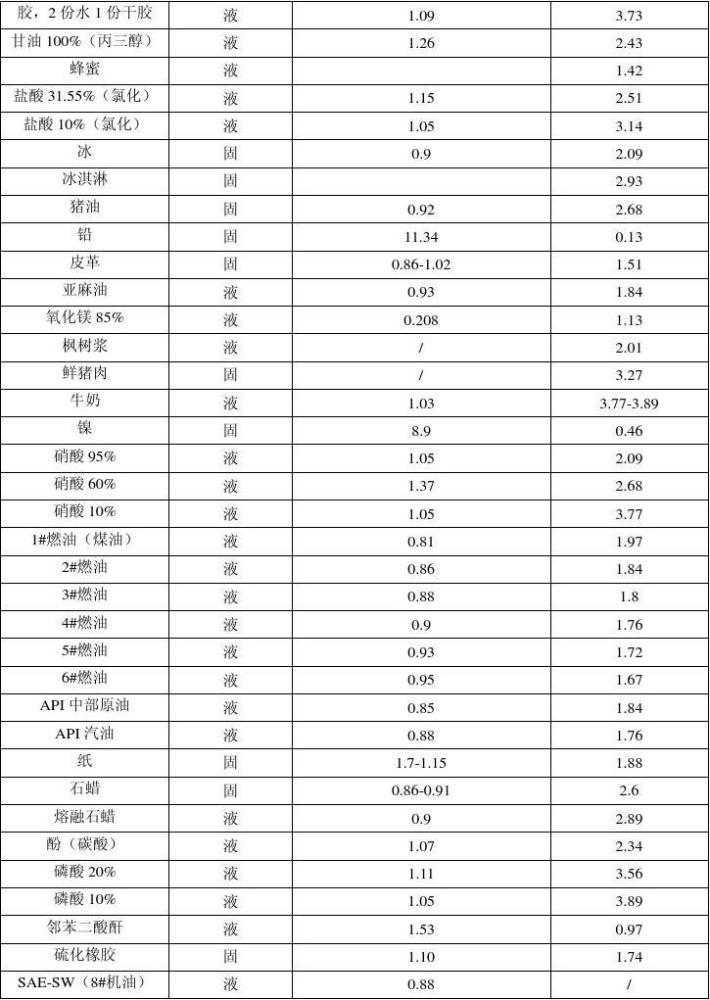
理论上说,常见液体和固体物质中,水的比热容最大
对上表中数值的解释:
⑴比热此表中单位为 kJ/(kg·℃)/ J/(kg·℃),两单位为千进制1kJ/(kg·℃)/=1×10³J/(kg·℃)
⑵水的比热较大,金属的比热更小一些
⑶c铝>c钢>c铁>c铅
补充说明:
1.不同的物质有不同的比热容,比热容是物质的一种特性,因此,可以用比热的不同来(粗略地)鉴别不同的物质(注意有部分物质比热相当接近)。
2.同一物质的比热一般不随质量、形状的变化而变化。如一杯水与一桶水,它们的比热相同,即比热容为强度性质。
3.对同一物质,比热值与物态有关,同一物质在同一状态下的比热是一定的(忽略温度对比热的影响),但在不同的状态时,比热是不相同的。例如水的比热与冰的比热不同。
4.在温度改变时,比热容也有很小的变化,但一般情况下可以忽略。比热容表中所给的比热数值是这些物质在常温下的平均值。
5.气体的比热容和气体的热膨胀有密切关系,在体积恒定与压强恒定时不同,故有定容比热容和定压比热容两个概念。但对固体和液体,二者差别很小,一般就不再加以区分。
常见气体的比热容
(单位:kJ/(kg·K))
Cp Cv
氧气0.909 0.649
氢气14.05 9.934
水蒸气1.842 1.381
氮气1.038 0.741