-
MAPK 编辑
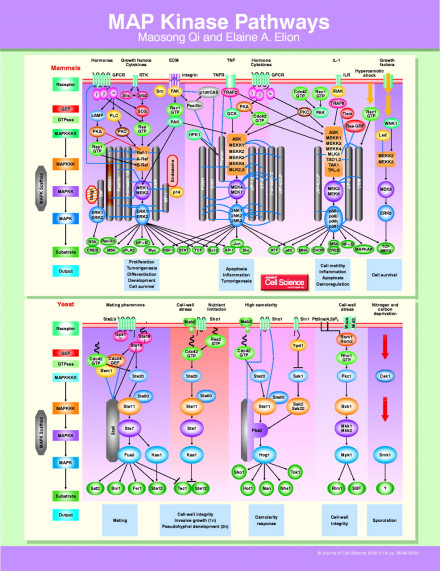
MAPK是信号从细胞表面传导到细胞核内部的重要传递者。已在哺乳动物细胞中鉴定了14种MKKK,7种MKK和12种MAPK。分析显示,这些激酶属于不同亚族。
MKKK
MKKK的4个亚族已得到鉴定,其中Raf亚族研究的最为透彻,包括B-Raf、A-Raf、Raf1。MEKK亚族由4种MEKK(MEKK1~MEKK4)构成。ASK1和Tpl2组成了MKKK的第三个亚族。第四个亚族与上述三个有较大不同,它包括MST(mammalian sterile 20-like)、SPRK、MUK(MAPK upstream kinase)、TAK1,以及相关程度最小的MOS(molony sarcoma oncoprotein)。
MKK
对于MKK来说,MEK1与MEK2密切相关,而MKK3则与MKK6密切相关。
MAPK
MAPK可分为4个亚族:ERK、p38、JNK和ERK5。这些通路由它们而得名,例如利用JNK的MAPK通路被称为JNK通路。
在哺乳动物中发现的第一个丝裂原活化蛋白激酶是ERK1(MAPK3)。由于ERK1及其近亲ERK2(MAPK1)均参与生长因子信号传导,因此该家族被冠名“丝裂原激活”。随着其他MAPK成员的发现,越来越明确这个名字是一个误称,因为大多数MAPK实际上参与对潜在有害的非生物应激刺激(高渗透压、氧化应激、DNA损伤、低渗透压)的反应。哺乳动物ERK1/2激酶作为细胞增殖调节剂的作用不是一般的,而是高度特化的功能。
大多数MAPK具有许多共同的特征,例如依赖于两个磷酸化事件的激活、三层通路结构和类似的底物识别位点。这些是“经典”的MAPK。但是,也有一些古老的“离群”激酶,它们不具有双重磷酸化位点,仅形成两层通路,并且缺乏其他MAPK所需的底物结合特征。这些通常被称为“非典型”MAPKs。还不清楚这些非典型MAPKs是否形成与经典MAPKs相反的独立群体。
一级结构
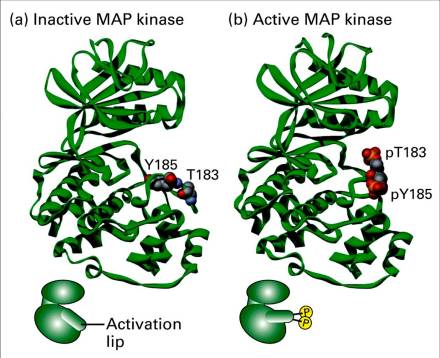
MKK都是通过双位点,即苏氨酸(T)和酪氨酸(Y)同时磷酸化激活MAPK。这两个磷酸化位点中间被一氨基酸隔开,构成三肽基TXY。不同的MAPK亚族成员,其双磷酸化位点之间的X残基不同,但是其各个亚族都具有标准的12个保守亚区,这些亚区是区分真核细胞蛋白激酶超家族的标志之一。MAPK家族成员之间具有较高的同源性。例如,p38β、p38γ和p38δ分别与p38α具有75%、62%和64%的同源性,而与其他MAPK家族成员的同源性约为40%~50%。三肽基位于蛋白激酶地VII和VIII亚区之间的Loop12环状结构内,该环位于分子表面并临近活性位点,其中部分残基形成一种唇状结构,被称为磷酸化唇或活化唇(activation lip)。这一区域被认为是决定包括MAPK在内的多种蛋白激酶活性的关键结构。二级和超二级结构
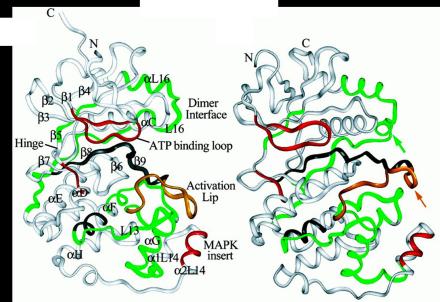
与其他蛋白激酶相似,ERK2、p38和JNK1都具有一个较小的氨基酸结构域和一个较大的羧基端结构域,两者之间由一个交叉区连接在一起。氨基酸结构域主要由β折叠组成,而羧基端结构域则主要为α螺旋,两个结构与交界处形成一个裂隙,为ATP结合位点。空间结构
大体结构:
p38与ERK2具有约40%序列同源性。将p38和ERK2的两个结构域同时重叠在一起时,其根均平方(root mean square ,RMS)偏离为0.17nm。JNK与ERK2和p38的同源性分别为40%和51%,其总体结构也与ERK2和p38非常相似。将ERK2和p38的羧基端结构域与JNK的羧基端结构域重叠式,两者较JNK3的羧基端结构域分别旋转了2.5°和4°。将ERK2的氨基酸和羧基端结构域与JNK3的对应结构域重叠时,其RMS偏离分别为0.115nm和0.158nm。
底物结合口袋的结构特征:
在所有MAPK中,形成底物结合口袋的氨基酸残基都是相当保守的。在未受到刺激时,ERK2的底物结合口袋被Arg192占据;当ERK2被磷酸化后,Arg192转离原来的位置,从而暴露出底物结合口袋来进行底物的结合。p38中,该位点活化机制尚不清楚。
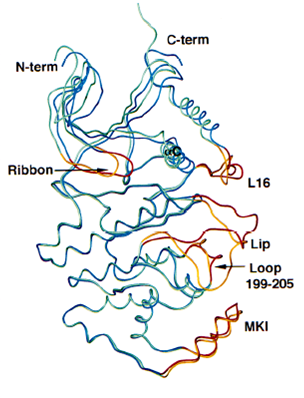 Superposition of ERK2 (green and gold)
Superposition of ERK2 (green and gold)
MAPK的活性被认为是由活化环的氨基酸序列中的双磷酸化位点所调控。MAPK活化环中的TXY序列是特定的MKK催化进行双磷酸化反应的位点。对于ERK/ERK2来说,双磷酸化位点是Thr183和Tyr185。这些位点的双磷酸化使MAPK的活性增加一千倍以上。
MAPK在它们的碱形式中是没有催化活性的。为了变得活跃,它们需要它们的活化环中发生(可能多个)磷酸化事件。这是由STE蛋白激酶组的专门酶进行的。
在经典MAP激酶的情况下,活化环包含一个特征性的TxY (苏氨酸-x-酪氨酸) motif (哺乳动物ERK1和ERK2中的TEY,ERK5中的TDY,JNK中的TPY,p38激酶中的TGY),为了把激酶结构域锁定在一个有催化活性的构象上,需要在苏氨酸和酪氨酸两个残基上都进行磷酸化。在体内和体外,酪氨酸的磷酸化常常先于苏氨酸的磷酸化,尽管任一残基的磷酸化都可以在没有另一残基的情况下发生。
这个串联活化环的磷酸化由Ste7蛋白激酶家族的成员,也就是MAP2激酶来执行。MAP2激酶又由许多不同的上游丝氨酸苏氨酸激酶(MAP3激酶)磷酸化激活。由于MAP2激酶在其同源MAPK以外的底物上显示非常小的活性,经典MAPK通路形成多层次,但相对线性的信号通路。这些信号通路可以有效地将刺激从细胞膜(在这里许多MAP3K被激活)传递到细胞核(只有MAPK可以进入核内)或许多其他的亚细胞靶点。
与三层的经典MAPK通路相比,一些非典型MAP激酶似乎具有更古老的两层系统。ERK3(MAPK6)和ERK4(MAPK4)最近被证明是被直接磷酸化的,因此被PAK激酶(与其他MAP3激酶相关)激活。与经典的MAP激酶相比,这些非典型MAPK只需要在它们的活化环中有一个残基被磷酸化。NLK和Erk7(MAPK15)激活的细节尚不清楚。
MAPKs的失活是由各种磷酸酶执行的。一个非常保守的专门磷酸酶家族是所谓的MAP激酶磷酸酶(MKP),它是双特异性磷酸酶(DUSP)的一个亚群。顾名思义,这些酶能够从磷酸酪氨酸和磷酸苏氨酸残基中水解磷酸基团。由于去除任一磷酸基团将大大降低MAPK活性,基本上消除信号,因此一些酪氨酸磷酸酶也参与灭活MAP激酶(例如,哺乳动物中的磷酸酶HePTP、STEP和PTRR)。
如上所述,MAPK通常形成多层通路,接收比实际MAP激酶高几层的输入。与MAPKs和MAP2Ks相对简单、磷酸化依赖的激活机制相比,MAP3Ks具有惊人的复杂调控。许多了解得更多的MAP3K,如c-Raf、MEKK4或MLK3,需要多个步骤来激活它们。这些酶通常是受变构效应控制的酶,通过多种机制紧密地锁定在非活性状态。激活它们的第一步是通过较小的配体(如c-Raf的Ras、MEKKK4的GADD45或MLK3的Cdc42)来减轻它们的自抑制。这通常发生在细胞膜上(但不总是),它们的大多数激活剂是结合在细胞膜上的(注意,由于异戊烯化修饰,小G蛋白是一直联系在细胞膜上的)。此步骤之后是“背靠背”的对它们可访问的激酶结构域的同源和异源二聚化。最近确定的复合物结构显示二聚体的形成方向使它们的两个底物结合区都自由。重要的是,这种二聚化事件还迫使MAP3激酶结构域采用部分活性构象。只有当这些二聚体在它们的活化环上相互磷酸化时,才能达到完全活性。后一步骤也可以通过辅助蛋白激酶(MAP4激酶,Ste20家族的成员)实现或辅助。一旦MAP3激酶完全激活,它可以磷酸化其底物MAP2激酶,这反过来又让MAP2激酶磷酸化它们的MAP激酶底物。
MAPK通路是细胞增殖、应激、炎症、分化、功能同步化、转化、凋亡等信号转导通路的共同交汇通路之一,把胞外信号经受体、G蛋白/小G、蛋白激酶、转录因子等组成的信号网络,传递到胞内,参与细胞增殖、分化、癌变、转移、凋亡等,不同的生长刺激、应激刺激,在不同的细胞.经不同细胞骨架局限的不同信号通路,可产生多种效应。MAPK的激活是细胞内磷酸化级联反应的最终步骤,经典的MAPK级联反应包括MAPKKKK(如Ras、Rho)一MAPKK激酶(MAPKKK)一将MAPKK丝氨酸/苏氨酸磷酸化一激活的MAPKK将MAPK的苏氨酸/酪氨酸双重磷酸化,激活MAPK。MAPK信号转导通路中存在的增强因子,可与MAPKKKs、MAPKKs和MAPKs结合,增加上游激酶对它们的激活能力。