-
牛病毒性腹泻-粘膜病 编辑
病原分类
迄今已经识别出至少17种不同亚型的BVDV-1(BVDV-1a至BVDV-1q),BVDV-2型又分为BVDV-2a、BVDV-2b、BVDV-2c和BVDV-2d4个亚型。BVDV-2型中BVDV-2a在全世界广泛分布基因型2b、2c和2d仅限于南美洲。在南美洲、北美洲和澳大利亚检测出了疑似BVDV的HoBi样病毒或称其为BVDV-3型病毒。
形态特征
BVDV基因组为单股正链RNA全长大约125kb,该基因组编码生成至少11种成熟的蛋白质,其中Capsid、E0、E1、E2、P7为病毒的结构蛋白,其余6种为非结构蛋白。BVDV感染细胞的类型、宿主趋向性与E2蛋白相关,但E2蛋白变异率比较高,导致BVDV能够逃脱宿主的免疫。
BVDV从生物型上可分为致细胞病变型和非致细胞病变型。致细胞病变型BVDV的产生是因为在其NS2/3蛋白编码序列发生了某些基因突变,包括基因重复,细胞mRNA序列插入和点突变这使NS2/3蛋白二聚体裂解为NS2和NS3单独的两个蛋白,这种改变导致BVDV变的能够杀死被感染的细胞。致细胞病变型BVDV通常是从持续感染的动物身上分离得到,这些动物的病情往往都已经发展到严重的粘膜病了。有研究显示,存在一些致细胞病变型的BVDV分离株这些分离株在Npro基因、衣壳蛋白基因及NS4b蛋白基因都存在基因突变。当致细胞病变BVDV突变后不再致病,按照其生物学特性改称其为非致细胞病变型BVDV。另外,根据BVDV基因组5'-NTR区差异可将其分为两种基因型,即BVDV-1和BVDV-2。由于单链基因组的性质BVDV具有较高的突变率,在一些情况下可导致新的病毒基因型的出现。
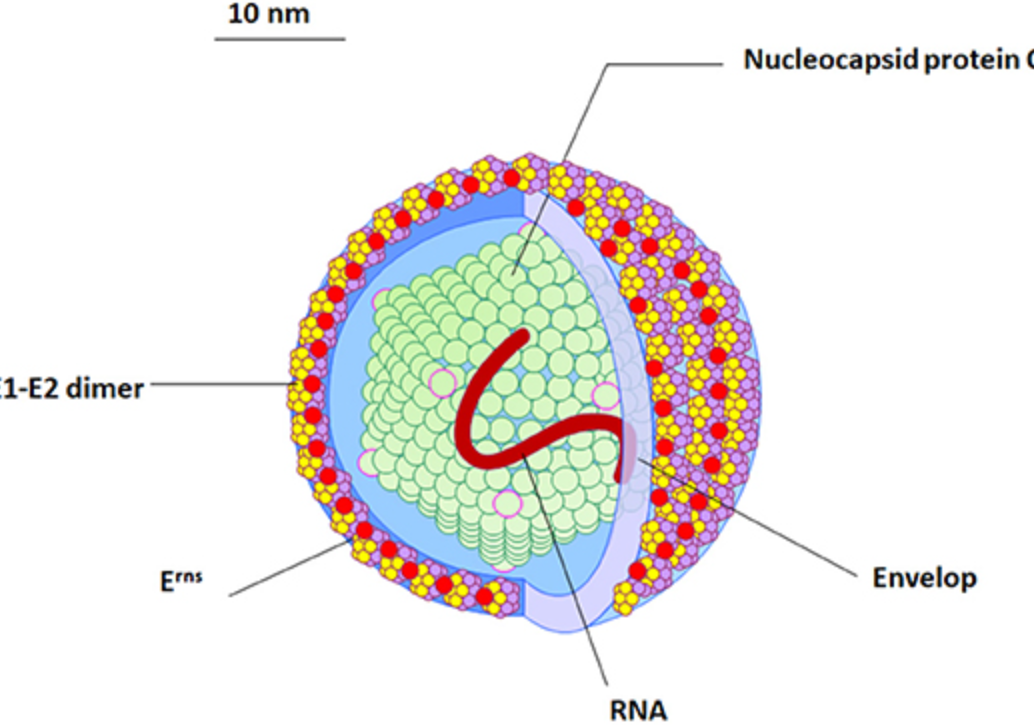 BVDV的基因组和形态结构示意图
BVDV的基因组和形态结构示意图
四种结构蛋白(蛋白C、Erns、E1和E2)包裹着RNA(红色)。病毒蛋白质外壳含有重要的E1-E2异二聚体,这是病毒进入所必需的。
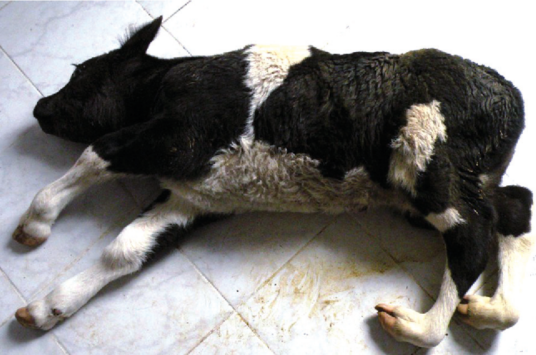
根据牛病毒性腹泻-粘膜病的严重程度和病程长短,在临床上该病可分为MD和慢性BVD,MD是致死性疾病综合征。临床症状为口腔糜烂、严重腹泻、脱水、白细胞减少和高热慢性BVD的特征是发病几周至几月后出现间歇腹泻,口鼻、趾间溃疡和消瘦。
急性BVD是一种普通类型,发生于正常牛,感染后产生的高效价抗体将病毒从体内消除,临床上为隐性型和温和型经过。此型病牛发病中,血清中病毒的浓度含量及含病毒的白细胞百分比明显低于持续感染牛(P1牛)。BVDV引起胚胎早期死亡,重新吸收、流产、木乃尹化、先天异常和死胎。无临床症状的P1牛,无明显的胃肠道粘膜和淋巴组织的肉眼可见及镜检变化:中性白细胞和淋巴细胞机能在P1牛中下降。某些P1牛出现早产、生长阻滞、哺乳困难、对疾病抵抗能力降低。
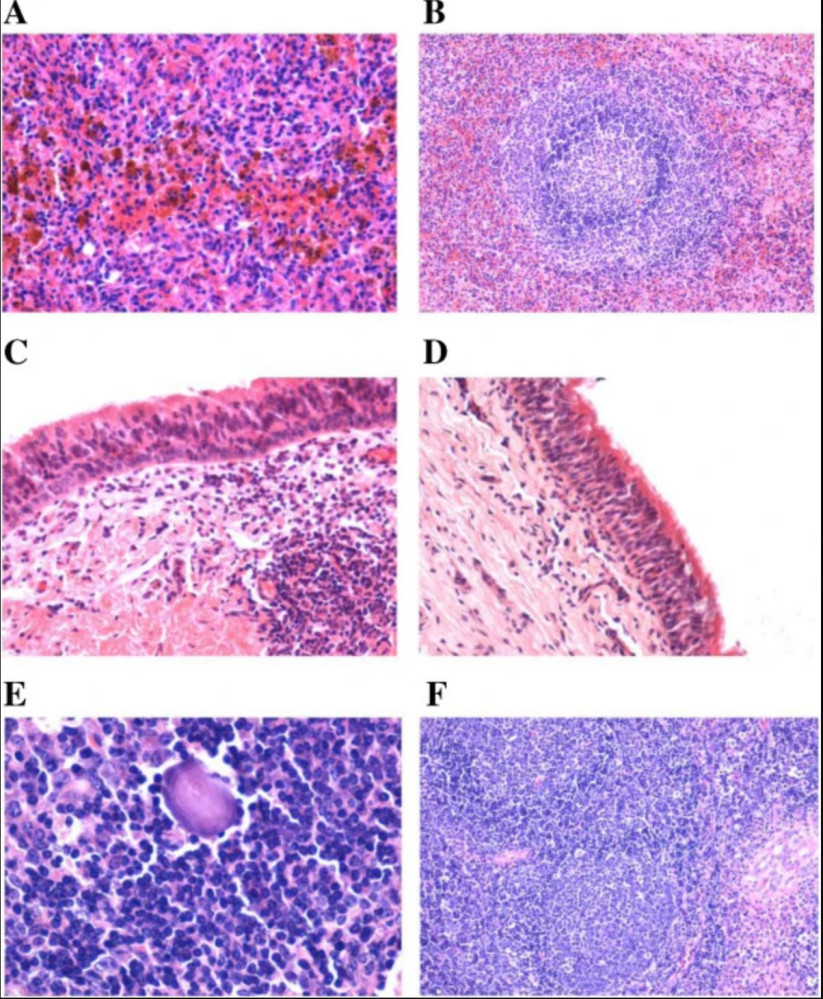
(A)脾红髓出血,含铁血黄素巨噬细胞明显增(B)控制正常(C)部分气管粘膜上皮肿胀;固有层中有中性粒细胞和浆细胞浸润;淋巴细胞增生;淋巴滤泡增多(D)控制正常(E)巨噬细胞和网状细胞增生增多(F)控制正常。
传染源
病畜和带毒动物是牛病毒性腹泻(BVD)的主要传染源。病畜的分泌物、尿液、血液、精液和流产胎儿等均可引起牛场BVD的发生现在认为持续感染牛(PI)是引起BVD发病的主要来源
传播途径
BVDV可通过水平传播和垂直传播感染宿主BVDV可通过呼吸道和消化道传播,也可通过胎盘交配和人工授精直接传染易感动物。BVDV能通过胎膜屏障进入胎儿体内,产出的胎儿为PI牛,终身带毒、排毒。持续感染会导致流产、胎儿死亡、卵泡功能不全等繁殖性疾病,并且会导致奶牛产量下降,免疫抑制进而导致疾病的协同并发。检测和清除PI牛是防治本病的重点与难点。
传播特点
BVD多呈地方性流行和季节性流行,在封闭集约化养殖场多以暴发式发病。此病在新疫区急性病例多,老疫区很少发生,多呈隐性感染发病率和病死率很低。BVD在一年四季均可发生但在冬未和春季多发。
但由于该病没有独特的病理变化和临床症状,引起腹泻和消化道粘膜糜烂或溃疡的疾病较多,因此临床诊断较困难,确诊需进行实验室诊断。中国外学者已建立了众多诊断检测方法。
病毒分离鉴定
病毒分离鉴定技术是确诊BVD的基本方法之。BVDV可以在牛睾丸或牛肾细胞(MDBK)上生长而MDBK细胞是BVDV培养最常用的细胞。病畜的全血、排泄物、血清、脾脏和肠系膜淋巴结等都可以分离到病毒,但该方法对试验条件要求较高不适合大规模的病毒检测和流行病学调查
电镜观察
电镜技术很少用于BVD的诊断但在病原学研究方面,电镜观察是其研究的常用技术之一。将新鲜病料或细胞培养物直接进行负染或者做成超薄切片通过电镜观察病毒粒子形态特征进行诊断。赵月兰等1251将BVDV分离株用磷钨酸负染在电镜下观察病毒形态结构显示病毒粒子直径为40~60纳米形态略呈圆形与BVDV颗粒基本一致
血清学诊断方法
血清学诊断方法中最常用的是酶联免疫吸附试验(ELISA)包括检测抗体的间接ELISA和检测抗原的抗原捕获ELISA等。此外病毒中和试验(VNT)和免疫荧光技术(IFA)也可用于检测BVDV。在实验室检测中,病毒中和试验和抗原捕获ELISA是最常用的检测技术,该方法符合OIE推荐的病原检测方法要求。
分子生物学技术
分子生物学技术在实验室应用最多的是耳组织或血液样品的RT-PCR和实时荧光定量RT-PCR检测实时荧光定量PCR具有特异性高、敏感性强快速和重复性好等优点,同时实时荧光定量RT-PCR的灵敏度比RT-PCR的高100倍。根据BVDV国际标准株基因序列,在其最保守的5端非编码区序列设计合成一对特异性引物经PCR扩增鉴定扩增后产物还可用于后续基因的测序和分析鉴定。此外BVDV单克隆抗体技术也可用于BVDV的诊断。
预防措施
首先要做好环境卫生管理,其次做好免疫预防工作最后对疑似感染牛进行隔离和药物治疗如果发现持续性感染的牛应立即淘汰针。
对中国BVD的流行情况建议首先做好分子流行病学的调查确定BVDV的基因类型方便后续药物和疫苗的有效使用。其次必须对进出口动物及生物制品进行严格的检疫,并加强中国兽用生物制品BVDV污染监测以及畜群BVDV净化工作。欧美等国家已经启动了国家和区域性的BVDV防控和根除计划并取得了显著效果。最后建立和健全BVDV检测体系尤其要检测并清除PI牛。加强预防工作对畜群进行特异性的的疫苗接种,并改进饲养管理及兽医防疫制度。
疫苗使用
BVDV疫苗包括常规疫苗和新型疫苗,而常规疫苗又分为弱毒苗、灭活苗和联合疫苗新型疫苗又分为亚单位疫苗、DNA疫苗和利用卡介苗作为载体进行研究的新型疫苗。
弱毒疫苗存在一个安全性的问题,弱毒苗比死苗或灭活苗的危险性更大,因为弱毒苗需要考虑其恢复致病力的可能性。
传统疫苗存在种种不足之处,迫使大量学者将精力投入到新型疫苗的研制当中。S.Harpin等成功构建了含有BVDVE2基因的重组质粒将该质粒接种小鼠后,可诱导小鼠产生特异性抗体抗体可存在6个月之久。S.Harpin等将构建的DNA疫苗以裸体的DNA疫苗(N-DNA)和脂质体包裹的疫(L-DNA)两种形式免疫牛结果表明:两者都可产生中和抗体。
而重组卡介苗的研究表明,卡介苗作为细菌活载体比利用重组病毒活载体更为方便,且适用范围更广,生产过程更简单稳定性更强。因此利用卡介苗作为载体进行新型疫苗的研究会成为一个热点。