-
微管 编辑
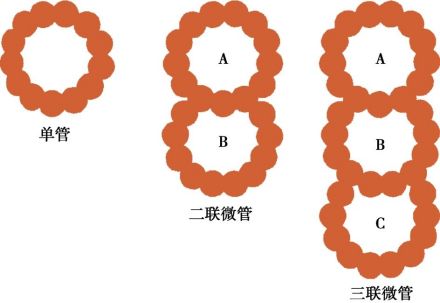
见于散在于细胞质中的、组成有丝分裂器的以及神经元中的微管等,大部分细胞质性的微管都属单微管。除后者外,这类微管易受低温、Ca和秋水仙素影响而解聚。
2.二联微管:
见于纤毛或鞭毛的周围微管,由并列相连的两管(亚丝)构成,对低温、Ca和秋水仙素较不敏感,但在超声波或高压处理时仍会解聚。
3.三联微管:
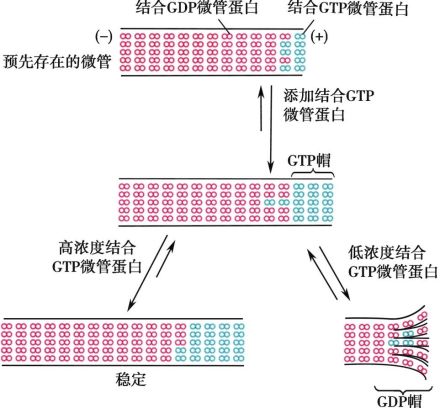
微管的组装是指由微管蛋白二聚体组合成微管的特异性和程序性过程。相反,由微管解离成为微管蛋白二聚体的过程称去组装。微管在适当条件下或在进行功能活动时,组装与去组装状态在细胞内可相互转换,以达到微管在数量及分布等方面的动态平衡。
微管的组装可分为延迟期、聚合期和稳定期三个时期。延迟期(1ag phase)又称成核期(nucleation phase),在该期α和β微管蛋白首先聚合成短的寡聚体(oligomer)结构——核心形成,紧接着二聚体在其两端和侧面大量增加,使之扩展成片状带,当片状带加宽至13根原纤维时,随即卷曲、合拢成一段原始的微管。由于该期是微管聚合的开始,速度较慢,为微管聚合的限速过程,故称为延迟期。聚合期(polymerization phase)又称延长期(elongation phase),该期中细胞内游离微管蛋白的浓度高,使微管的聚合速度大于解聚速度,新的二聚体不断加到原始微管的正端,使微管延长;直至游离的微管蛋白浓度下降,则解聚速度逐渐增加。在稳定期(steady STATe phase),胞质中游离的微管蛋白达到临界浓度,微管的组装(聚合)与去组装(解聚)速度相等。体外组装
Weisenbery实验室于1972年首次从小鼠脑组织中分离出微管蛋白,并在体外装配成微管。微管的体外组装需达到以下条件:①微管蛋白浓度(1mg/mL)。②必需有Mg2+和GTP存在。③最适pH值为6.9。④温度为37℃,α和β微管蛋白就可在体外组装成微管。若温度低于4℃或加入过量Ca2+,则使已形成的微管解聚为二聚体。体外组装,微管和微丝一样有踏车行为。体内组装
微管在体内的组装与去组装在时间和空间上是高度有序的。间期细胞中,胞质内微管和微管蛋白亚基库处于相对平衡状态;有丝分裂期中,胞质内微管的组装与去组装受细胞周期的调控,如在分裂前期,胞质内的微管处于去组装状态,可使游离的微管蛋白亚基组装为纺锤体,而分裂末期则发生相反的变化。微管聚合通常从特异性的核心形成位点开始,这些核心形成位点主要是中心体、鞭毛和纤毛的基体,称为微管组织中心(microtubule organizing center,MTOC)。大多数情况下,微管的正端远离微管组织中心,指向细胞边缘、轴突远端、鞭毛和纤毛顶部等,而负端总是指向微管组织中心。MTOC不仅是微丝组装的特异性的核心,而且还确定了微管的极性及微管中原纤维的数量。
微管的特异性药物在微管结构和功能的研究中发挥了重要的作用。秋水仙素和长春花属生物碱(长春花碱,长春新碱)等一些能与微管结合的药物,可抑制微管的聚合;而紫杉醇(pacilitaxel)可促进微管的聚合,并稳定已形成的微管。
秋水仙素(colchicine)是最重要的微管工具药物,用低浓度的秋水仙碱处理活细胞,可破坏纺锤体的结构。秋水仙素与Ca2+、低温、高压等因素直接破坏微管的作用机制不同,它可与二聚体结合,而结合有秋水仙素的微管蛋白组装到微管末端,可阻止其他微管蛋白的加入,从而阻断微管蛋白组装成微管。在细胞遗传学中,常用秋水仙素来制备中期染色体。
长春碱与二聚体结合的位点不同于秋水仙素,长春碱与二聚体的结合可稳定微管蛋白分子,从而增加二聚体与秋水仙素的结合。长春碱因具有阻止微管聚合,抑制微管形成的作用,在临床上常用于抗癌治疗。
紫杉醇与重水(D2O)一样可促进微管的组装,并增加微管的稳定性,抑制微管去组装。但它们所致的微管稳定性增加对细胞是有害的,导致染色体不能移动分离,使细胞周期停止于有丝分裂期。
微管具有聚合和解聚的动力学特性,在维持细胞形态、细胞分裂、信号转导及物质输送等过程中起着重要作用。生理情况下,细胞的结构、细胞器的定位和功能取决于微管结构的稳定程度。具体如下:
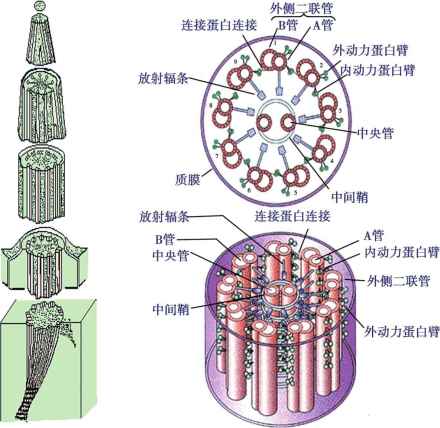
1、微管组成了鞭毛和纤毛,促成了它们的运动。构成鞭毛和纤毛的微管结构是“9+2”型,即外周由9对二联管(每对含有一个A亚丝,一个B亚丝)组成,中间有一对微管。在二联管A亚丝上有两种蛋白——连接蛋白和动力蛋白,连接蛋白与相邻的B亚丝永远相连,动力蛋白则与相邻的B亚丝时而连接,时而分开。动力蛋白由一个盘状的附着在A亚丝上的基部和3个柔软的头部含有ATP水解酶的结构组成。造成鞭毛和纤毛运动的根本是A、B亚丝之间在动力蛋白辅助下的滑动。2、微管参与神经细胞内递质的传递,参与细胞内小泡以及色素的运输,对细胞器如线粒体、核糖体定位有一定的支持作用。
3、微管组成纺锤体,在细胞分裂时染色体的运动上起重要作用。
4、在早期胚胎的形态发生过程中,微管起决定作用。
5、微管与其他纤维一起构成细胞骨架,微管双螺旋结构支撑着细胞生理形态,其自身不会发生收缩,因而可以维持细胞的生理形态。
6、微管具有传递重要信息的作用,例如重要生物学功能的微管信号转导,现如今此信号通道的研究很多,且已证实微管参与蛋白激酶信号转导功能,微管之间或者微管蛋白之间通过相互作用后,进一步传递着信号分子。