-
纤维蛋白溶解系统 编辑
血液凝固过程中形成的纤维蛋白被分解液化的过程,叫纤维蛋白溶解 fibrinolysis(简称纤溶)。纤溶活性异常增强,即纤溶亢进。纤溶亢进又分为原发性纤溶亢进和继发性纤溶亢进,可致出血。血纤维蛋白溶酶作用于纤维蛋白元或纤维蛋白,能将其多肽链的赖氨酸结合部位切断使之溶解的现象。由此产生的分解产物为FDP。纤溶过程也称血液凝固的第四相。
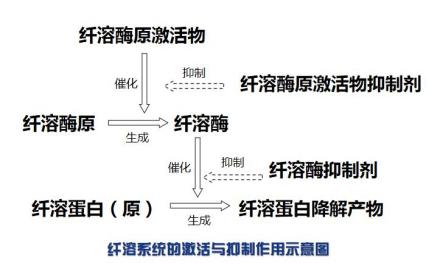
纤溶的激活物(纤溶酶原和纤维蛋白溶解酶即纤溶酶)和抑制物以及纤溶的一系列酶促反应,总称为纤溶系统。
血浆中抑制纤维蛋白溶解的物质统称为纤溶抑制物。它们存在于血浆、组织及各种体液中。根据其作用可分为两类:一类是抑制纤溶酶原激活,称为抗活化素;另一类是抑制纤溶酶的作用,称为抗纤溶酶。目前,临床上已广泛应用的止血药,如凝血酸、止血芳酸和6-氨基己酸等,就是抑制纤溶酶生成及其作用的药物。
在正常情况下,血液中的抗纤溶酶的含量高于纤溶酶的含量,因而纤溶酶的作用不易发挥。但在血管受损发生血凝块或血栓后,由于纤维蛋白能吸附纤溶酶原和激活物而不吸附抑制物,因而纤溶酶大量形成和发挥作用,使血凝块或血栓发生溶解液化。(1)组织型纤溶酶原激活物(t-PA):t-PA是一种丝氨酸蛋白酶,由血管内皮细胞合成。t-PA激活纤溶酶原,此过程主要在纤维蛋白上进行。
(2)尿激酶型纤溶酶原激活物(U-PA):u-PA由肾小管上皮细胞和血管内皮细胞产生。U-PA可以直接激活纤溶酶原而不需要纤维蛋白作为辅因子。
(3)纤溶酶原(PLG):PLG由肝脏合成,当血液凝固时,PLG大量吸附在纤维蛋白网上,在t-PA或u-PA的作用下,被激活为纤溶酶,促使纤维蛋白溶解。纤溶酶原是一个单链的β-球蛋白,分子量约为80000~90000。它在肝、骨髓、嗜酸粒细胞和肾中合成,然后进入血液中。成年人含量为10~20mg/100ml血浆。它在血流中的半衰期为2~2.5天。很容易被它的作用底物-纤维蛋白所吸附。
(4)纤溶酶(PL):PL是一种丝氨酸蛋白酶,作用如下:降解纤维蛋白和纤维蛋白原;水解多种凝血因子Ⅴ、Ⅷ、Ⅹ、Ⅶ、Ⅺ、Ⅱ等;使纤溶酶原转变为纤溶酶;水解补体等。
(5)纤溶抑制物:包括纤溶酶原激活抑制剂(PAI)和α2抗纤溶酶(α2-AP)。PAI能特异性与t-PA以1:1比例结合,从而使其失活,同时激活PLG.主要有PAI-1和PAI-2两种形式。α2-AP由肝脏合成,作用机制:与PL以1:1比例结合形成复合物,抑制PL活性;FⅩⅢ使α2-AP以共价键与纤维蛋白结合,减弱了纤维蛋白对PL作用的敏感性。
(6)纤维蛋白原(Fg):是参加止血、血栓形成的主要物质,纤维蛋白凝块又是血栓的主体。由于其分子量比较大,且易在血液中形成网状结构,所以又与血浆粘度有密切关系。正常值为2-4g/L。Fg增高时血液粘度增大,产生血栓的可能性也加大,在动脉壁受损和动脉粥样硬化(AS)时,Fg可在其表在上沉积。Fg是血栓性疾病独立的危险因素。
(1)纤溶酶原激活途径:PLG可通过三条途径被激活为PL,分别为内激活途径、外激活途径和外源激活途径。
(2)纤维蛋白(原)降解机制:PL不仅降解纤维蛋白,而且可以降解纤维蛋白原。PL降解纤维蛋白原产生X片段、Y片段及D、E片段。降解纤维蛋白则产生x'、Y'、D-D、E'片段。上述所有的片段统称为纤维蛋白降解产物(FDP)。
纤维蛋白溶解的基本过程可分为两个阶段:纤溶酶原的激活与纤维蛋白的降解。
1.纤溶酶原的激活
正常情况下,血浆中纤溶酶原无活性。只有在激活物的作用下,它才能转变成具有催化活性的纤溶酶。纤溶酶原的激活物存在于血液、各种组织和组织液中,也可由微生物产生。主要有三类:
(1)血管激活物 血管激活物在小血管的内皮细胞中合成后,释放入血。如血管内出现血凝块,它可使血管内皮细胞释放大量这种激活物,并被吸附于血纤凝块上面。肌肉运动,静脉阻塞,儿茶酚胺与组织胺等也可使血管内皮细胞合成与释放这种激活物增加。
(2)组织激活物 组织激活物存在于很多种组织细胞中,以子宫、甲状腺和淋巴结等组织中含量最高,肺和卵巢次之。正常时,组织激活物存在于细胞内,当组织受损时释放入血,促使纤溶酶原变为纤溶酶。如临床病人,如实施某些器官手术后,常易发生渗血现象。又如妇女的月经血也不凝固,都与这些组织内,含有丰富的组织激活物有关。
(3)尿激活物 尿液中含有纤溶酶原激活物,称尿激酶。它是肾脏及泌尿道上皮细胞释放的。此外,在胆汁、唾液、乳汁、脑脊液、羊水、腹水、关节腔液中,均含有激活物原或激活物。这些激活物都具有防止纤维蛋白栓塞,保持管腔通畅的生理作用。
某些细菌也含有激活纤溶酶原的物质。如链球菌中含有链激酶,葡萄球菌中含有葡激酶,故机体感染这些细菌后,均可激活纤溶酶原成为纤溶酶。
2.纤维蛋白的降解
纤溶酶是血浆中活性最强的蛋白酶,但其特异性较差。它可以水解肽链上各个赖氨酸-精氨酸相连接的部位,从而逐步将整个纤维蛋白或纤维蛋白原的分子,分割成很多可溶性的小肽(蛋白质碎片),这些小肽统称为纤维蛋白降解产物。此降解产物一般不再凝固。
血管内出现血栓时,纤溶作用主要局限于血栓发生处,而不扩展到周围血液。这可能是由于血浆中有大量抗纤溶物质(即抑制物)和血栓中的纤维蛋白分子可吸附或结合大量纤溶酶激活物所致。
6-氨基己酸 (epsilon aminocaproic acid,EACA)
1953年合成,1964年用于心脏手术,半衰期较短。EACA通过可逆地结合纤溶酶原上的赖氨酸结合位点,阻断纤溶酶原与纤维蛋白上的赖氨酸结合,抑制纤溶酶原转变为纤溶酶,大剂量时可直接抑制纤溶酶,从而减少CPB后出血和输血量。在不同研究中,EACA有不同的剂量应用方案,一般而言,推荐的成人标准剂量方案是150mg/kg作为静脉注射负荷量,继之以15mg/(kg·h)术中维持输入。
多数文献认为在CPB前预防性使用EACA能够有效抑制CPB期间纤溶系统的激活,使术后出血减少,并减少术后输血量。进一步研究表明EACA对减少心瓣膜置换术患者术后出血的有效性虽不及抑肽酶,但并不增加术后输血量。在对进行初次CABG患者的研究中则发现,与使用安慰剂相比,EACA不仅可以减少术后出血以及输血量,且无过敏反应,不增加中风、认知功能障碍、肾功能不全、心肌梗塞、血栓形成和桥闭塞等并发症的发生率。而与使用抑肽酶相比,EACA在抑制纤溶系统激活及减少术后出血方面并无明显差异。
在OPCABG的相关研究中则发现EACA虽可抑制术后纤溶亢进,但并不能减少术后出血量。总之,多数研究认为在减少术后出血和输血方面,EACA有与抑肽酶相似或稍弱的效能,临床结果并无明显统计学差异。
氨甲环酸 (Tranexamic Acid,AMCA)
AMCA是临床广泛应用的一种赖氨酸同类物抗纤溶药,作用强度是EACA的5~10倍。1964年合成,1988年首次用于CPB心脏手术。AMCA除了能可逆地结合纤溶酶原上的赖氨酸结合位点抑制纤溶酶原转变为纤溶酶外,也能通过阻止纤溶酶诱发的血小板激活而减少出血。AMCA的应用剂量从10~20g不等,随剂量增加并不能进一步减少术后出血量。目前普遍认为,CPB前预防性应用AMCA能有效减少心脏手术患者围术期出血和异体血的需要量,减少术后并发症和改善预后。但是对于是否可以减少因出血而致的再次手术发生率,各研究结果不一。AMCA的给药时间与CPB开始的关系会影响其作用。在对CABG患者的随机双盲研究中,采用相同剂量AMCA在CPB前给予或CPB后给予,并与安慰剂对比,结果发现在CPB后给予AMCA并不能显著减少术后出血量和异体输血需要量,临床作用有限。MAngano等的一项关于心脏手术抗纤溶药物效果比较研究显示,AMCA在预防心脏围手术期失血的效果与抑肽酶类似,但不良反应和造成的终末器官损害的风险比抑肽酶低,对抑肽酶的安全性提出质疑,并推荐用AMCA替代抑肽酶作为防止心脏手术失血的药物。
进一步研究表明,进行主动脉瓣置换(AVR)的患者,AMCA在减少输血方面与抑肽酶无异,而对于CABG患者,AMCA则略逊于抑肽酶,从而认为AMCA对于有高输血风险的手术的作用有限。在对血小板功能的保护方面,抑肽酶则优于AMCA。但是,也有研究表明AMCA在保护CPB后血小板功能方面与抑肽酶并无差异。这也许与实验采用不同方法对血小板功能进行评价有关。关于心脏手术中使用抗纤溶药物风险的研究则表明,实施初次瓣膜手术及高风险手术的患者在使用AMCA后,癫痫发作的比例较使用抑肽酶的明显增高。同时,实施初次瓣膜手术的患者,持续房颤以及肾功能衰竭的发生也较抑肽酶组高。而在实施初次CABG的患者群中则发现,使用抑肽酶的患者急性心肌梗塞及肾功能不全的发生较AMCA组高,此外,在实施高风险手术的患者中,术后1年死亡率,抑肽酶组也明显高于AMCA组,由此建议抑肽酶应避免使用于CABG及实施高风险手术的患者,实施瓣膜手术的患者则应避免使用AMCA。在OPCABG患者中的研究同样发现AMCA可减少术后出血以及血制品的使用。
AMCA的不良反应比较少见,主要有恶心、腹泻,偶见有强直反应。临床应用未发现使用AMCA会增加血栓形成的概率。
氨甲苯酸 (Aminomethylbenzoic Acid.PAMBA)
1963年合成. 因1964年合成了作用更强的AMCA。国外应用PAMBA的报道较少,国内的一些研究显示,PAMBA能抑制CPB中纤溶系统激活,保护血小板功能,减少术后出血,无不良反应发生。
研究发现,在心脏手术中预防性应用大剂量抑肽酶PAMBA(20 mg/kg)可部分抑制CPB中的纤溶亢进。两者抗纤溶和减少首次手术出血量的作用相近。在PAMBA对CPB中血小板功能的保护作用研究表明,止血芳酸与抑肽酶在CPB中的保护血小板、防止其活化的作用相似,手术后出血量比较也无显著差异。
使用抗纤溶药物的风险及未来研究展望
当纤溶系统被抗纤溶药物抑制时极容易发生血栓栓塞,特别是对于那些本身存在动脉硬化基础病变而又需要进行心脏手术的患者。由于抑肽酶可导致术后严重肾功能衰竭、心肌梗死或心力衰竭、中风等不良事件发生率增高,目前临床已禁止使用。而赖氨酸同类物是人工合成的抗纤溶药物,由于其结构简单,无明显的不良反应,而且不会影响ACT测定,鲜有血栓形成的相关报道,就目前的研究来看可以作为停用抑肽酶后心脏手术中血液保护的替代药品。
然而不容忽视的是,赖氨酸同类物在预防围手术期失血的应用没有像抑肽酶那么广泛,参与科学评估的样本数量和次数比抑肽酶要少得多,因而现在还不能对其安全性太过信任。而且赖氨酸同类物在预防围手术期失血的疗效方面也没有像抑肽酶那样肯定。因此,在今后的研究中,需要对其安全性及有效性进行进一步评估,尤其是其在高风险手术中应用的安全性及有效性。此外,作为广谱丝氨酸蛋白酶抑制剂,抑肽酶除了有减少出血的作用,尚有抗炎、心肌保护及肺保护等功能,而赖氨酸同类物是否也具有上述作用,还需进一步证实。
抗纤溶药物在手术中有一定的减少围术期出血及输血量的作用,但由于其本身性质所在,也不可避免的带来血栓栓塞及心、脑、肾等重要脏器的损害的风险。因而,在临床上使用此类药物需权衡利弊,尤其是在有血栓栓塞风险的患者。