-
体液免疫 编辑
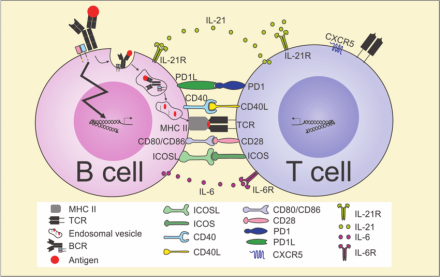
第一步:B细胞表面的受体分子与互补的抗原分子结合后,活化、长大,并迅速分裂产生一个有同样免疫能力的细胞群——克隆(clone)、无性繁殖系。其中一部分成为浆细胞,产生抗体;一部分发展为记忆细胞(memory CELL)。
第二步:需要巨噬细胞和Th细胞的参与。Mφ表面带有MHCⅡ分子,它们吞噬入侵的病原体,抗原分子经Mφ处理后表达在细胞膜上,夹在MHCⅡ分子的沟中。Th细胞表面带有不同的受体,能识别Mφ表面MHC+特异的抗原分子结合物。B细胞表面带有MHC分子,可和特异的抗原分子结合,Th细胞可刺激结合Ag的B细胞分化。这一步比第一步作用更强大。浆细胞(效应B细胞) 浆细胞产生抗体。浆细胞一般停留在各种淋巴结。每一个浆细胞每秒钟能产生2000个抗体,它们寿命很短,经几天大量产生抗体之后就死去,而抗体则进入血液循环发挥生理作用。浆细胞产生的抗体“Y”两短臂末端高变区与抗原结合,抗体的柄端(FC)可与吞噬细胞(如巨噬细胞)上的受体结合而使抗原—抗体复合物被吞噬。
记忆细胞 记忆细胞与二次免疫反应,记忆细胞不能分泌抗体,只能通过产生浆细胞,由浆细胞产生抗体。它们寿命长、对抗原十分敏感,能“记住”入侵的抗原。
当同样抗原第二次入侵时,能更快的做出反应,很快分裂产生新的浆细胞和新的记忆细胞,浆细胞再次产生抗体消灭抗原。这就是二次免疫反应。它比初次反应更快,也更强烈。
体液免疫的两个关键
产生高效而短命的浆细胞,由浆细胞分泌抗体清除抗原.
产生寿命长的记忆细胞,发生二次反应立即消灭再次入侵的同样抗原。
临床上一个反复发作的化脓感染,常使医生想到患者是否有免疫缺陷病,一般原发免疫缺陷发病年龄很小,而继发性免疫缺陷病人多在30岁以上。绝大多数免疫缺陷病人多表现为体液和细胞免疫同时受损,所以应全面检查这两方面的功能。遗憾的是,目前应用的检测方法的局限性,其结果常难以得出明确结论。
免疫球蛋白
血清免疫球蛋白(Ig)的测定是检查体液免疫功能最常用的方法。由于目前还没有发现由IgD和IgE缺陷所致疾病,所以通常检测IgG、IgM、IgA,这三类Ig就可以代表血清Ig的水平(表20-2)。检测发现三类Ig水平均明显低下,就可考虑体液免疫缺陷。但在分析儿童Ig水平时,应注意Ig的水平随年龄而变化。体液免疫功能缺陷首先考虑患者血清Ig水平,如果所有类别Ig水平均降低,即称为一般性联低丙种球蛋白血症。如果免疫球蛋白水平极度低下,或IgG、IgM、IgA,三类Ig总量低于2mg/ml则称为严重低丙种球蛋白血症或无丙种球蛋白血症(agammaglobulinemia)。如果只一种或两种Ig水平降低,则称为异常丙种球蛋白血症(dysgammaglobulinemia)。
一般性低丙种球蛋白血症多见于继发性免疫缺陷病。无丙种球蛋白血症常见于原发免疫缺陷病。但是常有约50%IgA缺陷病人无临床症状,伴有反复感染的IgA缺陷病人常同时有IgG的缺陷。常规的定量检测血中Ig的方法是单向免疫扩散和免疫比浊法。
2、分泌型IgA(SIgA)的测定
SIgA是粘膜抗感染的重要因素,但是粘膜抗感染还包括少量渗出的IgM和IgG,还有细胞免疫的作用。由SIgA缺陷病人常可检测出针对牛奶或其他食物蛋白的沉淀抗体和自身抗体,说明机体对抗原蛋白质吸收异常,同时也存在免疫调节系统的功能紊乱。一般来说血清IgA缺陷病人常伴有SIgA缺陷,反之亦然。说明在机体中血清IgA和SIgA之间有某种生物相关性。
最近也有报导少数SIgA缺陷病人的血清IgA水平正常,因而分别检查血清中和分泌液中IgA水平还是有必要的。目前用免疫比浊法可较精确地测定分泌液中IgA时和IgM和IgC水平。在用单向免疫扩散和免疫比浊法定量IgA时,因抗血清是针对这两型共有的α链的,故不能区分SIgA和血清来源的IgA。而应用抗分泌小体的抗体用酶免疫分析法,可区分血清IgA和分泌型IgA,并可对SIgA进行定量。
3、常见抗体的测定
检测体液免疫功能的另一种方法是定量测定正常人体内的几种常见的抗体水平。常见的抗体通常是指嗜异性凝集素、抗溶血素O抗体以及麻疹病毒、脊髓灰质炎病毒的抗体。
在严重免疫缺陷病人缺乏上述抗体,常见抗体的缺损可验证或支持免疫蛋白测定的结果。然而对于比较复杂的免疫缺陷,由于这类抗体主要反映过去的免疫应答能力,此外这种初次应答能力持续期短,易于消退,所以对新近发生的继发性免疫缺陷的诊断帮助不大。
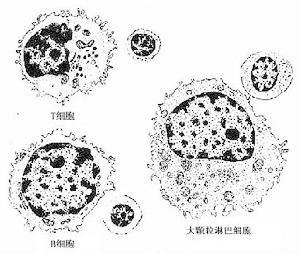
B细胞
原发性免疫缺陷和继发性免疫缺陷均可导致体液免疫功能下降。原发性体液免疫功能缺陷可能由于B细胞分化障碍,细胞内合成Ig功能紊乱或由于抑制性细胞功能过强。继发性体液免疫功能降低可能由于蛋白质大量丢失,蛋白质吸收障碍、营养不良、免疫抑制治疗的副作用,病毒感染(艾滋病)等。在诊断原发性体液免疫功能缺损中可检查B细胞的数目和功能以确定造成缺损的原因。
1.外周血B细胞数目的检测首先进行常规的外周血白细胞总数和分类计数检查,这些结果是评价病人免疫系统功能状态的基本资料。由于在全血中淋巴细胞所占比例很少,而T细胞和B细胞不能藉形态学特征分类,所以外周血B细胞数检测需先从全血分离出富含淋巴细胞的单个核细胞(peripheral blood moNOnuclear cell,PBM)。再依靠B细胞表面有免疫球蛋白分子或其他特征来检查B细胞。常用的方法是将待检者的PBM用FITC标记的免疫抗人Ig作直接免疫荧光染色,在荧光显微镜下显荧光的细胞为带有表面免疫球蛋白的B细胞。正常人B细胞的约占PBM的10%。
2.外周血B细胞功能的检测 分离受检者血液PBM细胞,体外培养时加入B细胞刺激物如RWM(美洲商陆刺激素)或SAC(金黄色莆萄球菌来源的刺激物)后由B细胞变成Ig分泌细胞的数量。体液免疫功能缺损患者,其PBM对PWM和SACA刺激的反应降低,产生Ig分泌细胞数正常人显著减少。在进一步检查这种免疫缺损的原因,则应检查是由B细胞或TH细胞缺损所致,还是由于TS细胞数量或活性增强引起的。
抗体形成细胞计数:检查人类Ig分泌细胞是用反向溶血空斑检测(reversed hemolytic plaque assay)法。将待检人的PBM、用SPA包被的SRBC(SPA-SRBC)、兔抗人Ig抗体、补体四种成分混合,灌入用两张玻片做成的小室,密封好,放入温箱培养1-3小时,,在此期间,作为抗人Ig抗体的免疫IgG的FC段可与SRBC表面SPA结合,当Ig分细胞分泌出游离的Ig分子时,这些人Ig分子与SRBC表面的抗人Ig抗体结合形成免疫复合物,即可活化补体,使SPA-SRBC溶解,因此在Ig分泌细胞周围形成一个圆形的溶血区,称为溶血空斑,每一个溶血的空斑就代表一个Ig分泌细胞。
检查小鼠Ig分泌细胞应用的溶血空斑试验比较简单,即SRBC免疫注射小鼠,4天后取脾制成单个细胞悬液,加入一定量SRBC(靶细胞)混合,在补体参加下,产生抗体的细胞分泌出的Ig与SRBC(抗原)结合在补体作用下,溶血,表现肉眼可见的溶血空斑。计数空斑数代表分泌抗体的细胞数。
体液免疫是一个相当复杂的连续过程,大体上可以分为三个阶段。
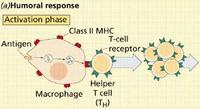
感应阶段
抗原进入机体后,除少数可以直接作用于淋巴细胞外,大多数抗原都要经过吞噬细胞的摄取和处理,经过处理的抗原,可将其内部隐蔽的抗原决定簇暴露出来。然后,吞噬细胞将抗原呈递给T细胞,刺激T细胞产生淋巴因子,淋巴因子刺激B细胞进一步增殖分化成浆细胞和记忆细胞。少数抗原可以直接刺激B细胞。
反应阶段
B细胞接受抗原刺激后,开始进行一系列的增殖\分化,形成效应B细胞。在这个过程中,有一小部分B细胞成为记忆细胞,该细胞可以在体内抗原消失数月乃至数十年以后,仍保持对抗原的记忆。当同一种抗原再次进入机体时,记忆细胞就会迅速增殖、分化,形成大量的效应B细胞,继而产生更强的特异性免疫反应,及时将抗原清除。
效应阶段
在这一阶段,抗原成为被作用的对象,效应B细胞产生的抗体可以与相应的抗原特异性结合,发挥免疫效应。例如,抗体与入侵的病菌结合,可以抑制病菌的繁殖或是对宿主细胞的黏附,从而防止感染和疾病的发生;抗体与病毒结合后,可以使病毒失去侵染和破坏宿主细胞的能力。在多数情况下,抗原抗体结合后会发生进一步的变化,如形成沉淀或细胞集团,进而被吞噬细胞吞噬消化,等等。
指B细胞在T细胞辅助下,接受抗原刺激后形成效应B细胞和记忆细胞。效应B细胞产生的具有专一性的抗体 与相应抗原特异性结合后完成的免疫反应。体液免疫的关键过程是产生高效而短命的效应B细胞,由效应B细胞分泌抗体清除抗原。产生寿命长的记忆细胞,在血液和淋巴中循环,随时“监察”,如有同样抗原再度入侵,立即发生免疫反应以消灭之(二次反应)。
细胞免疫
指T细胞在接受抗原刺激后形成效应T细胞和记忆细胞.效应T细胞与靶细胞特异性结合,导致靶细胞破裂死亡的免疫反应。
免疫功能
而且还相互配合共同发挥免疫效应。病毒感染过程中,往往是先通过体液免疫来阻止病毒在机体内传播,若病毒已经侵染到寄主细胞中,就要通过细胞免疫.这是效应T细胞与靶细胞结合,使靶细胞通透性改变,渗透压发生变化,最终导致靶细胞破裂死亡。
胞内寄生物
体液免疫先起作用,阻止寄生物的散播感染;当寄生物进入细胞后细胞免疫将抗原释放;再由体液免疫最后清除。若细胞免疫不存在时,体液免疫也将大部分丧失。
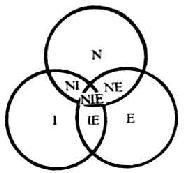
机体内各系统可抽象地以集合概念表明,则神经,免疫和内分泌三系统间的关系可以图10-1中的集合群表示。其中三个集合两两重叠处可分别代表神经(N)与免疫(I),免疫(I)与内分泌(E)及神经(N)与内分泌(E)间的共同范畴,而三重叠部应视为神经、免疫和内分泌的共同内容(NIE)。集合间各有种组合方式可罗列如表10-1和图10-2。
图10-1神经(N)、免疫(I)和内分泌(E)系统的关系
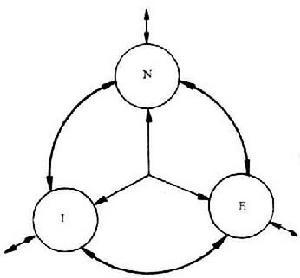
图10-2N、I、E间作用方式由表10-1可见,神经免疫内分泌学(NIE)与神经内分泌学(NE)、神经免疫学(NI)和免疫内分泌学(IE)相比,涉及更为复杂的系统间影响和作用。内内涵广泛,并以NE、NI和IE间的联系为基础。系统间作用方式,既有直接和间接之分,亦要同时和先后之别,系统间交互作用的性质可为增强、减弱、修饰、允许或协同,借变频、变时和变力等方式体现。系统间作用的属性,可有生理和病理性之分,是质和量的互变过程。上述关系图示为二维描述,实际应为立体过程,结合时间变量,则三大系统间的交互影响即为四维图象,这难以直观图示。
鉴于描述神经,免疫和内分泌系统间关系的术语较多且易混淆,缺乏统一性,故应确定术语的范畴及相互关联系,以决定相应学科内容及领域。
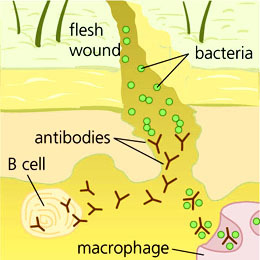
当抗原(病菌或病毒)第一次感染人体时,会被先天免疫的细胞所吞噬、清除,而其中一部分细胞特称APC——在刺激B细胞方面主要为树状细胞(dendritic cells),APC抗原递呈现细胞(antigen.presenting cell),它们除了能吞噬、分解抗原,还能将分解后的碎片(一小段peptides)呈现(present)给B cell,使之活化、分裂,并经clonoal seleCTion(细胞细选择、株落选择)节选出对抗原最具亲和力的抗体,(此时为lgm),抗体的变异区(variable region)能与抗原产生专一性的结合,阻止它感染正常细胞,并用另一端的FC portion与巨噬细胞结合,使巨噬细胞吞噬抗原,达到消菌的目的。
活化的B细胞在过一段时日(通常大于四周)后会把分泌的抗体由lgm转变为lgG。lgG在人体的寿命远较lgm长,约六个月。受过第一次刺激的B细胞在四周后变为记忆B细胞(memory cells),除了分泌lgG外,它还能在第二次感染时以更快的时间产生更多的抗体,同时,memory B cell在人体特定抗原的感染而言是具有终身的保护作用的。这也是打疫苗能保护一个人免疫受特定病菌感染的原因。
在现代内分泌学的理论体系中,“内分泌”概念应包括内分泌、神经内分泌、旁分泌和自分泌等方式;而激素的内涵亦大为增加,诸如局部激素、循环激素、神经激素等,而许多免疫因子如淋巴因子和单核因子等均符合激素的标准;严格地讲,神经系统和免疫系统既与内分泌系统有种种区别,又有诸多共性,这也是系统间相互影响的基础。表10-1N、I、E间的作用和联系方式及相应学科划分。
细胞免疫和体液免疫是借助于血液循环、淋巴循环或组织液而进行和实现的生理过程,而神经内分泌调控也最终由循环血液或组织液完成,故在此交汇路途上难免发生交叉性影响和作用。所以神经内分泌或免疫内分泌联系在活体内必将受到免疫或神经源性因素的影响。已研究的神经免疫学领域和内容,绝大多数发现有内分泌因素或成份的参与。精神和心理活动以及行为的共同基础是中枢神经系统的高级功能活动,由此可把精神神经免疫学(psychoneuroimmunology)及行为神经免疫心理学(behaviouralneuroimmunololgy)划入神经免疫内分泌学(neuroimmunoendocrinology),作为其重要的分支学科。
神经免疫内分泌学可直接引用神经科学、免疫学和内分泌学的相关概念和理论,其研究方法应是跨学科的,研究工作应采用多重指标,全面观察,对相关临床问题的考察,更应从多方面入手,分清主次矛盾,并应考虑与其它系统的联系和影响,以期在不同水平上全面而完整地反映机体的真实生理过程。