-
内质网 编辑
内质网由KR.Porter等于1945年发现,他们在观察培养的小鼠成纤维细胞时,发现细胞质内部具有网状结构,建议叫做内质网(endoplasmic reticulum,ER),后来发现内质网不仅仅存在于细胞的“内质”部,通常还有质膜和核膜相连,与高尔基体关系密切,且常伴有许多线粒体。
内质网(ER)是细胞质内由膜组成的一系列片状的囊腔和管状的腔,彼此相通形成一个隔离于细胞基质的管道系统,为细胞中的重要细胞器。实际上是一个连续的膜囊和膜管网,可分为粗面内质网(rough endoplasmic reticulum,RER)和滑面内质网(smooth endoplasmic reticulum,SER)两大部分(粗面内质网也称为糙面内质网或颗粒型内质网,滑面内质网也称为光面内质网或非颗粒型内质网)。
内质网联系了细胞核和细胞质、细胞膜这几大细胞结构,使之成为通过膜连接的整体。内质网负责物质从细胞核到细胞质,细胞膜以及细胞外的转运过程。
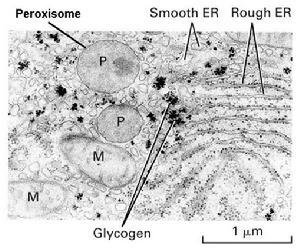
粗面内质网
主要形态特征为网膜胞质面有核糖体颗粒附着,并由此得名。粗面内质网在形态上多为排列整齐的扁囊,在功能上,主要与外输性蛋白质及多种膜蛋白的合成、加工及转运有关。因此,在具有分泌肽类激素或蛋白质功能的细胞中,粗面内质网发达,如胰腺细胞、浆细胞等。在未分化或低分化的细胞中相对不发达,如胚胎细胞、肿瘤细胞等。
滑面内质网
电镜下呈光滑的小管、小泡样网状结构,常与粗面内质网相通。滑面内质网是一种多功能的细胞器。在不同细胞、同一细胞的不同发育阶段或不同生理时期,其形态结构、数量、细胞内空间分布及发达程度差异较大,而且常表现出不同的功能特性。如睾丸间质细胞、卵巢黄体细胞及肾上腺皮质细胞中有大量的滑面内质网,是与其合成类固醇激素的功能有关;肝细胞中丰富的滑面内质网与其减毒功能有关;在平滑肌和横纹肌中的滑面内质网特化为肌质网,通过储存及释放Ca2+调节肌肉收缩。
两种类型的内质网在不同组织类型的细胞中分布状况不同。有的细胞只有粗面内质网,如胰腺细胞;有的只有滑面内质网,如肌细胞;还有些细胞中二者以不同比例共存,而且随着细胞的不同发育阶段或生理功能状态的变化发生类型转换。
内质网除上述两种基本类型外,在某些特殊组织细胞中存在一些由内质网局部特化、衍生而来的异型结构。如视网膜色素上皮细胞中的髓样体(myeloid body),在生殖细胞、快速增殖细胞、某些哺乳类动物神经元和松果体细胞,以及一些癌细胞中出现的孔环状片层体(annulate lamellae)等。
ER膜中磷脂占50%~60%,蛋白质约占20%,脂类主要成分为磷脂,磷脂酰胆碱含量较高,鞘磷脂含量较少,没有或很少含胆固醇。ER约有30多种膜结合蛋白,另有30多种位于内质网腔,这些蛋白的分布具有异质性,如葡萄糖-6-磷酸酶,普遍存在于内质网,被认为是标志酶,核糖体结合糖蛋白(ribophorin)只分布在RER,p450酶系只分布在SER。
内质网是细胞质的膜系统,外与细胞膜相连,内与核膜的外膜相通,将细胞内的各种结构有机地联结成一个整体,有效地增加细胞内的膜面积,具有承担细胞内物质运输的作用。
ER主要功能是合成蛋白质和脂类,分泌性蛋白和跨膜蛋白都是在ER中合成的。ER合成的脂类除满足自身需要外,还提供给高尔基体、溶酶体、内体、质膜、线粒体、叶绿体等膜性细胞结构。滑面内质网上没有核糖体附着,所占比例较少,但功能较复杂,它与脂类、糖类代谢有关,参与糖原和脂类的合成、固醇类激素的合成以及具有分泌等功能。在胃组织的某些细胞的滑面内质网上曾发现有CI的积累,这说明它与HCl的分泌有关。在小肠上皮细胞中,可以观察到它与运输脂肪有关。在心肌细胞和骨骼肌细胞内的滑面内质网与传导兴奋的作用有关,在平滑肌细胞内,与Ca2的摄取和释放有关。粗面内质网上附着有核糖体,其排列也较滑面内质网规则,功能是合成蛋白质大分子,并把它从细胞输送出去或在细胞内转运到其他部位。蛋白质合成旺盛的细胞,粗面内质网发达。在神经细胞中,粗面内质网的发达与记忆有关。光滑型内质网的功能与糖类和脂类的合成、解毒、同化作用有关,具有运输蛋白质的功能。这两种内质网的比例与细胞的功能有着密切的联系,如胰腺细胞中粗面型内质网特别发达,这与胰腺细胞合成和分泌大量的胰消化酶蛋白有关,在睾丸和卵巢中分泌性激素的细胞中,则滑面型内质网特别发达,这与合成和分泌性激素有关。细胞质中内质网的发达程度与其生命活动的旺盛程度呈正相关。电镜下,内质网是由单位膜构成的扁囊(池)和小管,并互相通连。粗面内质网由扁囊和附着在其外表面的核糖体构成,表面粗糙,细胞核周围的粗面内质网可与核膜外层通连。主要功能是合成分泌蛋白质。滑面内质网表面光滑无核糖体附着,主要参与类固醇、脂类的合成与运输,糖代谢及激素的灭活等。
蛋白质加工
蛋白质都是在核糖体上合成的,并且起始于细胞质基质,但是有些蛋白质在合成开始不久后便转在内质网上合成,这些蛋白质主要有:
②跨膜蛋白,并且决定膜蛋白在膜中的排列方式;
③需要与其它细胞器组合严格分开的酶,如溶酶体的各种水解酶;
④需要进行修饰的蛋白,如糖蛋白。
C. Milstein(1972)发现从骨髓瘤细胞提取的免疫球蛋白分子N端要比分泌到细胞外的N端多出一段。G. Blobel和D. Sabatini等根据进一步的实验,提出了信号假说(Signal hypothesis),认为蛋白质上的信号肽,指导蛋白质转至内质网上合成。Blobel因此项发现获1999年诺贝尔生理医学奖。
蛋白质转入内质网合成至少涉及5种成分:
①信号肽(signal peptide),是引导新合成肽链转移到内质网上的一段多肽,位于新合成肽链的N端,一般16~30个氨基酸残基,含有6-15个带正电荷的非极性氨基酸,由于信号肽又是引导肽链进入内质网腔的一段序列,又称开始转移序列(start transfer sequence)。
②信号识别颗粒(signal recognition particle,SRP),由6种结构不同的多肽组成,结合一个7S RNA,分子量325KD,属于一种核糖核蛋白(ribonucleoprotein)。SRP与信号序列结合,导致蛋白质合成暂停。
③ SRP受体(SPR receptor),是膜的整合蛋白,为异二聚体蛋白,存在于内质网上,可与SRP特异结合。
④停止转移序列(stop transfer sequence),肽链上的一段特殊序列,与内质网膜的亲合力很高,能阻止肽链继续进入内质网腔,使其成为跨膜蛋白质。
⑤转位因子(translocator),由3-4个Sec61蛋白复合体构成的一个类似炸面圈的结构,每个Sec61蛋白由三条肽链组成。
蛋白质转入内质网合成的过程:
信号肽与SRP结合→肽链延伸终止→SRP与受体结合→SRP脱离信号肽→肽链在内质网上继续合成,同时信号肽引导新生肽链进入内质网腔→信号肽切除→肽链延伸至终止→翻译体系解散。这种肽链边合成边向内质网腔转移的方式,称为cotranslation。
一些信号肽序列的蛋白质及信号序列
Preproalbumin
Met-Lys-Trp-Val-Thr-Phe-Leu-Leu-Leu-Leu-Phe-Ile-Ser- Gly-Ser-Ala-Phe-Ser↓Arg...
Pre-IgG light chain
Met-Asp-Met-Arg-Ala-Pro-Ala-Gln-Ile-Phe-Gly-Phe-Leu- Leu-Leu-Leu-Phe-Pro-Gly- Thr-Arg-Cys↓Asp...
Prelysozyme
Met-Arg-Ser-Leu-Leu-Ile-Leu-Val-Leu-Cys-Phe-Leu- Pro-Leu-Ala-Ala-Leu-Gly↓Lys...
蛋白质的修饰与加工
包括糖基化、羟基化、酰基化、二硫键形成等,其中最主要的是糖基化,几乎所有内质网上合成的蛋白质最终被糖基化。
糖基化的作用是: ①使蛋白质能够抵抗消化酶的作用;②赋予蛋白质传导信号的功能;③某些蛋白只有在糖基化之后才能正确折叠。
糖基一般连接在4种氨基酸上,分为2种:
O-连接的糖基化(O-linked glycosylation):与Ser、Thr和Hyp的OH连接,连接的糖为半乳糖或N-乙酰半乳糖胺,在高尔基体上进行O-连接的糖基化。
N-连接的糖基化(N-linked glycosylation):与天冬酰胺残基的NH2连接,糖为N-乙酰葡糖胺。
内质网上进行的为N-连接的糖基化。糖的供体为核苷糖(nucleotide sugar),如CMP-唾液酸、GDP-甘露糖、UDP-N-乙酰葡糖胺等。糖分子首先被糖基转移酶转移到膜上的磷酸长醇(dolichol phosphate)分子上,装配成寡糖链。再被寡糖转移酶转到新合成肽链特定序列(Asn-X-Ser或Asn-X-Thr)的天冬酰胺残基上。
新生肽链的折叠、组装和运输
COP Ⅱ介导由内质网输出的膜泡运输,这种膜泡由内质网的排出位点(exit sites)以出芽的方式排出,内质网的排出位点没有结合核糖体,随机分布在内质网上。不同的蛋白质在内质网腔中停留的时间不同,主要取决于蛋白质完成正确折叠和组装的时间,这一过程是在属于hsp70家族的ATP酶的作用下完成的,需要消耗能量。有些无法完成正确折叠的蛋白质被输出内质网,转入溶酶体中降解掉,大约90%的新合成的T细胞受体亚单位和乙酰胆碱受体都被降解掉,而从未到达靶细胞膜。
其他功能
1.合成膜脂
大多数膜脂是完全在内质网中合成的,例外的情况包括:
①鞘磷脂是在内质网上开始合成的,但完成于高尔基体;
②某些线粒体和叶绿体独有的膜脂是驻留在这些细胞器中的酶催化合成的。ER合成的膜脂以膜泡运输的方式转运至高尔基体,溶酶体和质膜上,或借磷脂转移蛋白(phospholipid transfer protein,PTP)形成水溶性复合物,转至其他膜上。
2.解毒作用
SER中的p450酶系属于单加氧酶(moNOoxygenase),又称为多功能氧化酶 (mixed funCTion oxiDAse)、羟化酶(hydroxylase),因其还原态的吸收峰在450nm处,故此命名。主要分布在SER中,但也存在于质膜、线粒体、高尔基体、过氧化物酶体、核膜等细胞器的膜中,具有解毒作用,通常可将脂溶性有毒物质,代谢为水溶性物质,使有毒物质排出体外。有时也会将致癌物代谢为活性致癌物。p450种类繁多,但都是与其他辅助成分组成一个呼吸链来实现其功能,呼吸链中的P450还原酶实际就是一种黄素蛋白。p450催化O2分子中的一个原子加到底物分子上使之羟化,另一个氧原子被NADH或NADPH提供的氢还原生成水,在此氧化过程中无高能磷酸化合物生成。
3.甾体类激素的合成
在生殖腺和肾上腺的内分泌细胞中,SER、线粒体,可能还有高尔基体上的一些酶共同参与甾体类激素的合成。
4.调节血糖浓度
使葡糖6-磷酸水解为磷酸和葡萄糖,释放糖至血液中。细胞中的糖元可被酶转化为葡糖1-磷酸,再转变为葡糖6-磷酸,但由于膜对磷酸化的糖是高度不通透的,葡糖6-磷酸只有在去磷酸化以后才能通过质膜,进入血液。
5.形成一些特殊结构
如肌细胞中的SER特化成的肌质网可储存钙离子,作为细胞内信号物质。
6.支撑作用
内质网是细胞内最丰富的膜,形成了一种网络结构,提供机械支撑作用,并成为细胞质中酶附着的支架。
7.转送作用
内质网可通过出芽来运送合成物,其中光面内质网尤为突出。
细胞质的改变:滑面内质网和粗面内质网
滑面内质网
1、滑面内质网增生滑面内质网与产生固醇物质,解毒、激素灭活等功能有关,如解毒作用增强,肝细胞内滑面内质网增多,肾上腺皮质瘤内滑面内质网也多。
2、肌浆网水肿 肌浆网亦属滑面内质网,与肌肉收缩及钙离子释放回收有关。肌细胞缺氧,中毒时,肌浆网可出现水肿。
粗面内质网
1、粗面内质网扩张、囊泡化 正常粗面内质网系由膜形成扁池,腔很窄,在细胞水肿时,液体入腔内使之扩张,并形成小泡,在肝炎时肝细胞气球样变中也可见到。
2、粗面内质网脱粒 粗面内质网扁池膜旁有核糖体依附,在粗面内质网肿胀同时膜表面核糖体脱落。也有的粗面内质网膜表面核糖体脱落,但扁池不扩张。
3、粗面内质网板层 在内分泌细胞及胚胎肝细胞内出现短而紧密排列粗面内质网,在内分泌肿瘤及肝癌中也可见到。
4、同心圆膜性小体 有三种:第一种粗面内质网呈同心圆板层排列;第二种是滑面膜双层呈同心圆排列;第三种是在滑面间夹有糖原。
5、粗面内质网池内隔离 粗面内质网扁池扩张,带有核糖体的膜突入扩张的池内,切面如像岛状膜性小管小泡游离在池内。
6、粗面内质网对合池 平行两片粗面内质网紧密靠拢,内侧面核糖体消失。也可有三片或多片,称三合池或多合池。
内质网的应激反应,即在某些情况下,钙稳态失衡,出现错误蛋白质或未折叠蛋白质过度堆积、固醇和脂质等水平失调而启动的应激机制,从而影响特定基因表达。如果内质网功能持续紊乱,那么细胞就会最终启动凋亡程序。ER的应激反应简称ERS,大体可以分为未折叠蛋白应答反应(UPR)、内质网超负荷反应(EOR)、胆固醇调节级联反应(SREBP)三种。
未折叠蛋白应答反应(UPR)
哺乳动物细胞内有3种ER跨膜蛋白,它们分别是需要肌醇酶1(IRE1)、PKR类似的内质网激酶(PEKR)、活性转录因子6(ATF6),它们在URP途径中共同协作完成反应过程。它们在正常条件下均与调控蛋白Bip/GRP78(以下以Bip举例)形成稳定复合物,在内质网蛋白质异常过度堆积后,它们与Bip解离,引发3条不同的途径执行UPR。
第一条途径最先发现于酵母菌当中,IRE1为跨膜蛋白,膜外与Bip结合,膜内含有可以切割Hac1mRNA的部位(RNA内切酶活性)。过度蛋白质堆积的时候,Bip与IRE1分离与堆积的蛋白质结合,同时IRE1趋向于二聚体(二聚化)并交叉磷酸化,即两个单体各带有一个Pi分子。接着IRE1将Hac1mRNA的内含子切下,留下并连接外显子,外显子连接组成新的mRNA,进一步翻译形成转录因子Hac1,该因子进入核内激活编码ER分子伴侣的基因,新合成的ER分子伴侣协助蛋白质折叠,缓解危机。
第二条途径是PERK和IRE1类似地进行二聚化和交叉磷酸化,Bip与其解离。同时PERK使得翻译起始因子eIF2α发生磷酸化,使得后者不能完成GTP和GDP之间的交换作用,暂缓蛋白质的合成,对应激反应起到帮助作用。另外有研究表明此行为还会激活JNK,P38信号途径,通过转录因子如ATF4诱导相关基因上调。
第三条途径通过内质网跨膜蛋白ATF6完成的,它原本与 内质网膜共价结合,应激反应时先转入高尔基体,被S1P和S2P蛋白酶裂解激活,激活后的ATF6进入细胞核内,激活编码Bip/GRP78和XBP-1等基因,产生相应的mRNA进而进行调控。
EOR和SREBP反应
内质网超负荷反应(EOR)
细胞除了用UPR应对错误蛋白过度堆积于内质网,还会启动其他机制来应对紧急情况,比如激活细胞核因子NF-kB来引发EOR反应,最终产生对前炎性细胞因子,进而激活细胞存活、凋亡、细胞炎症反应和细胞分化等相关信号途径。
胆固醇调节级联反应(SREBP)
该反应主要涉及三种蛋白:固醇调控元件结合蛋白(SREBP)、insig-1(2)和SCAP。当胆固醇水平过高时,insig-1(2)和SCAP-SREBP复合物结合,将后者锚定在内质网膜上,抑制胆固醇的合成。当胆固醇水平降低时,SCAP-SREBP复合物被释放到高尔基体上,SREBP在两个位点被S1P和S2P蛋白酶切割,从而使SREBP的N端结构域bHLH得以释放,释放后的它称作核-SREBP,成为活性因子,进入核内调控靶基因。
ERS引发的细胞凋亡程序
在应激反应依然无法调节,持续的不平衡状态出现后,细胞会启动凋亡程序。一般认为细胞凋亡程序是和钙稳态失调引起的,而内质网的另一重要功能是储存钙离子。在ERS反应的某些信号刺激下,内质网膜上IP3R通道开放,致使大量钙离子外流,高水平的钙离子与需钙蛋白酶结合导致calpain酶原大小亚基水解而被活化,活化的calpain可以裂解多种蛋白质底物,比如裂解vinculin而破坏细胞骨架稳定性,使细胞凋亡,还可以剪切Bcl-xL使其由抗凋亡变为促凋亡。活化的calpain还可以转移至内质网,在几个切割位点切割caspase-12酶原,使其活化,作为细胞凋亡的重要水解酶而发挥作用。