-
自然杀伤细胞 编辑
自然杀伤细胞( natural killer cell,NK细胞)来源于骨髓淋巴样干细胞,其分化、发育依赖于骨髓及胸腺微环境,主要分布于骨髓、外周血、肝、脾、肺和淋巴结。NK细胞不同于T、B细胞,是一类无需预先致敏就能非特异性杀伤肿瘤细胞和病毒感染细胞的淋巴细胞 。
NK细胞确切的来源还不十分清楚,一般认为直接从骨髓中衍生,其发育成熟依赖于骨髓的微环境。小鼠和人的体外实验表明,胸腺细胞在体外IL-2等细胞因子存在条件下培养也可诱导出NK细胞。小鼠脾脏在体内IL-3诱导下可促进NK细胞的分化。NK细胞主要分布于外周血中,占PBMC 5~10%,淋巴结和骨髓中也有NK活性,但水平较外周血低。
由于NK细胞具有部分T细胞分化抗原,如80~90%NK细胞CD2+,20~30%NK细胞CD3+(表达CD3ζ链),30%NK细胞CD8+(α/α)和75~90%NK细胞CD38+,而且NK细胞具有IL-2中亲和性受体,在IL-2刺激下可发生增殖反应,活化NK细胞可产生IFN-γ,因此一般认为NK细胞与T细胞在发育上关系更为密切。与T细胞、B细胞相比,NK细胞表面标志的特异性是相对的。人NK细胞mIg-,部分NK细胞CD2、CD3和CD8阳性,表达IL-2受体β链 (P75,CD122),CD11b/CD18阳性。常用检测NK细胞的标记有CD16、CD56、CD57、CD59、CD11b、CD94和LAK-1。
一种稳定表达在NK和LAK细胞表面的LAK-1分子,120kDa,NK细胞在IL-2条件下培养20天LAK-1仍为阳性,而HNK-1(CD57)和CD16部分消失。LAK的杀伤活性可被抗LAK-1 McAb所抑制。
通过CD3分子的ζ链
NK细胞不表达TCR/CD3复合物,但部分NK细胞表达CD3ζ链,当用CD16抗体刺激NK细胞活化时,ζ链发生酪氨酸磷酸化,引起胞浆内Ca2+ 浓度升高,IP3水平增加,促进细胞因子合成和ADCC作用。
通过CD2分子
CD2与CD58相互作用或用CD2 McAb刺激可活化NK细胞,CD3 ζ链发生酪氨酸磷酸化。
自然杀伤细胞刺激因子
自然杀伤细胞刺激因子(natural killer cell stimulatory faCTor,NKSF) 对NK细胞有刺激作用。
IL-2、IL-12、IFN-α、TNF-α以及白细胞调节素(leukoregulin,LR) 对NK细胞的活化和分化有正调节作用, 体外培养时加入上述细胞因子可明显提高NK的杀伤活性。前列腺素 (PG)E1、E2、D2和肾上腺皮质激素等对NK细胞的活性有抑制作用。
NK细胞表面具有IL-2中亲和性受体,IL-2诱导NK的杀伤活性约需18~24小时。此外,IL-2还可诱导NK细胞的增殖,一般在刺激后3~4天开始发生增殖,其机理为IL-2可诱导NK细胞表达IL-2Rα链,新表达的α链与原先细胞表面的β链和γ链结合形成高亲和性受体,在IL-2存在下刺激NK细胞发生增殖。IL-2诱导NK细胞的活性机理尚不清楚,可能与增加细胞粘附分子的表达,提高对NK抵抗靶细胞的杀伤活性有关,还可能增加NK细胞胞浆中的颗粒以及丝氨酸酯酶mRNA的表达,活化和促进杀伤介质的杀伤作用。
自然杀伤活性
由于NK细胞的杀伤活性无MHC限制,不依赖抗体,因此称为自然杀伤活性。NK细胞胞浆丰富,含有较大的嗜天青颗粒,颗粒的含量与NK细胞的杀伤活性呈正相关。NK细胞作用于靶细胞后杀伤作用出现早,在体外1小时、体内4小时即可见到杀伤效应。NK细胞的靶细胞主要有某些肿瘤细胞(包括部分细胞系)、病毒感染细胞、某些自身组织细胞(如血细胞)、寄生虫等,因此NK细胞是机体抗肿瘤、抗感染的重要免疫因素,也参与第Ⅱ型超敏反应和移植物抗宿主反应。
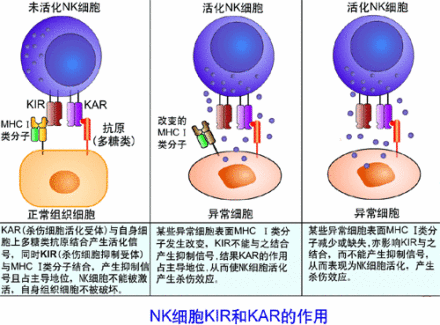
⒈ 识别靶细胞 NK细胞识别靶细胞是非特异性的,这与CTL识别靶细胞机理不同,但确切的机理尚未明了。现已知淋巴细胞功能相关抗原-1(LFA-1) 与靶细胞表面的细胞间粘附分子-1(ICAM-1)的作用参与NK细胞的识别过程,抗LFA-1或抗ICAM-1 McAb可抑制NK细胞的杀伤活性。此外CD2与LFA-3(CD58)结合以及CD56也可能介导NK细胞与靶细胞的结合。有关白细胞分化抗原和粘附分子分别参见第一章和第二章。
⒉ 杀伤介质 主要有穿孔素、NK细胞毒因子和TNF等。
⑴ 穿孔素: 穿孔素是一种由NK、CTL、LAK等杀伤细胞胞浆颗粒释放的杀伤靶细胞的介质,有关穿孔素的结构和功能参见本章第二节。从胞浆颗粒中纯化的穿孔素在体外能溶解多种肿瘤细胞,抗穿孔素抗体可抑制杀伤活性。IL-2可提高穿孔素基因的转录。IL-6可以促进IL-2对穿孔素基因转录的诱导作用。丝氨酸酯酶可能有活化穿孔素的作用。
⑵ NK细胞毒因子: NK细胞可释放可溶性NK细胞毒因子(NK cytotoxic factor,NKCF),靶细胞表面有NKCF受体,NKCF与靶细胞结合后可选择性杀伤和裂解靶细胞。
⑶ TNF:活化的NK细胞可释放TNF-α和TNF-β(LT),TNF通过①改变靶细胞溶酶体的稳定性,导致多种水解酶外漏;②影响细胞膜磷脂代谢;③改变靶细胞糖代谢使组织中pH降低;④以及活化靶细胞核酸内切酶,降解基因组DNA从而引起程序性细胞死亡等机理杀伤靶细胞。TNF引起细胞死亡过程要明显慢于穿孔素溶解细胞的作用过程。
NK细胞表面具有FcγRⅢA,主要结合人IgG1和IgG3的Fc段(Cγ2、Cγ3功能区),在针对靶细胞特异性IgG抗体的介导下可杀伤相应靶细胞。IL-2和IFN-γ明显增强NK细胞介导的ADCC作用。以前认为在淋巴细胞中由K细胞介导ADCC,但仍未发现K细胞特异的表面标记,也不能证实K细胞是否属于一个独立的细胞群, 很可能NK是介导ADCC的一个主要淋巴细胞群。具有ADCC功能的细胞群除NK外,还有单核细胞、巨噬细胞、嗜酸性粒细胞和中性粒细胞。
分泌细胞因子
活化的NK细胞可合成和分泌多种细胞因子,发挥调节免疫和造血作用以及直接杀伤靶细胞的作用。
此外,NK细胞可抑制PWM体外诱导B细胞的 分化及抗体应答, 其机理可能通过直接抑制B 细胞或抑制辅佐细胞的抗原提呈作用。NK细胞通过自然杀伤和ADCC发挥的细胞毒作用,在机体抗病毒感染、免疫监视中起重要作用。⑴ 抗病毒感染: NK可选择性地杀伤病 毒感染的靶细胞。由辅佐细胞或NK细胞所产生 的IFN可协同NK的抗病毒作用, 而对正常细胞 有保护作用。另一方面,病毒感染细胞表面的 病毒抗原和其它表面分子使得其对NK的杀伤细 胞作用变得更加敏感。在体外,NK可溶解疱疹病毒、牛痘病毒、麻疹病毒、腮腺炎病毒、巨细胞病毒和流感病毒感染的靶细胞。体内试验表明, NK低活性小鼠品系对某些病毒感染更加敏感;注射抑制NK细胞的抗Asialo GM1抗体可加重小鼠流感病毒性肺炎。此外,NK细胞在体外还可杀伤某些细菌、真菌、原虫等,可能与NK细胞释放某些杀伤介质有关。⑵NK细胞在免疫监视、杀伤突变的肿瘤细胞可能比T细胞具有更重要的作用。某些疾病如Chediak-Higashi或X性联淋巴增殖综合征患者, 由于NK功能缺陷对恶性淋巴细胞增殖疾病特别易感。⑶参与骨髓移植后移植物抗白血病效应 (graft-versus-leukemia effECT,GVL): 在体外NK细胞可杀伤某些淋巴样和髓样白血病细胞。骨髓移植后数周内,来自供体的NK细胞在PBL中占相当高的比例。此外,在体内NK细胞还可杀伤某些不成熟细胞如骨髓干细胞、胸腺细胞亚群等。
自然杀伤细胞是一种细胞质中具有大颗粒的细胞,也称NK细胞。因为其非专一性的细胞毒杀作用而被命名。没有T细胞B细胞所具的受体,不会进行受体的基因重组。但仍具有一些特殊受体,可以活化或抑制其作用。占循环中淋巴细胞族群的5-10%。和杀死肿瘤细胞有关,可利用分泌穿孔素及肿瘤坏死因子,摧毁目标细胞。
自然杀伤细胞属于粒状淋巴细胞,是人体免疫系统的组成部分。它能迅速溶解某些肿瘤细胞,因此开发它的抗癌功能是近年来癌症研究的重点。
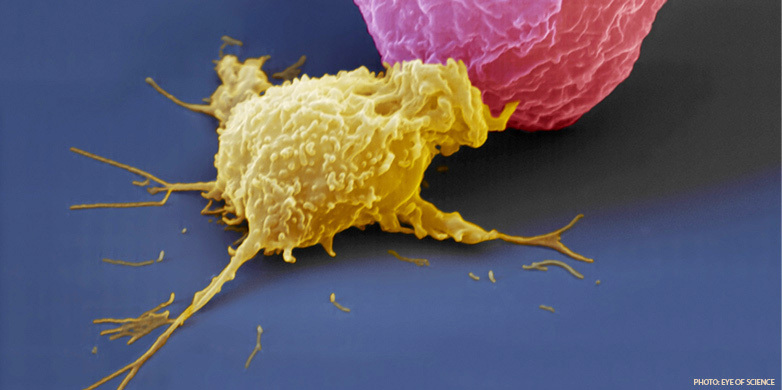
NK细胞为什么不攻击它的同伴,自然杀伤细胞(黄色)在它们严重破坏机体之前识别并杀死癌细胞(粉红色)或病毒感染的细胞。
人类的免疫系统是非常复杂的,它有着大量不同的细胞具有各种各样的功能,这确保侵入的微生物如病毒或细菌能够迅速地使之无害并保持整个机体的健康。
免疫系统还包括自然杀伤细胞(NK细胞),其识别并消除肿瘤或病毒感染的细胞。因此,NK细胞对抗人体自身的应激细胞以防止它们成为一个潜在的危险。然而,这种承担是有风险性的。其他的免疫细胞——特异性杀伤细胞,也被称为CD8 + T细胞,响应于病毒感染时不断地繁殖和变得成熟,也可以表现出应激症状,从而可能终结在NK细胞的名单上。
干扰素伪装免疫细胞
免疫生物学教授Annette Oxenius的研究小组发现,是什么阻止nk细胞杀死免疫系统的“来自于其他部门的同事”:健康CD8 +T细胞能够检测免疫信使物质1型干扰素,1型干扰素通过与这些免疫细胞的特定表面受体结合,从而隐藏它们的应激。换句话说,1型干扰素作为一种伪装斗篷使得免疫细胞不被NK细胞看见。如果T细胞缺乏1型干扰素的停泊位点,那么它们就会被NK细胞追杀直至灭绝。
使用感染两种模型病毒的小鼠,研究人员发现,如果动物的CD8 +t细胞缺乏这些干扰素的受体,不仅NK细胞消除感染病毒的细胞,而且免疫细胞也被认为采取了行动,从而削弱了抗病毒的免疫反应。
训练有素的细胞死亡信号
研究人员使用CD8 + T细胞没有任何1型干扰素受体的小鼠探索工作机制是如何运作的,以及缺乏1型干扰素的CD8 + T细胞是如何耗尽NK细胞的。如果没有自然杀手的存在,尽管缺乏干扰素检测,但T细胞依然会增多,成熟和发育。此外,瑞士苏黎世联邦理工学院的免疫生物学家发现,这些无需传感器的T细胞逐渐形成其表面的“识别标签”,一旦与NK细胞接触,就会引发NK细胞的杀伤作用。因此,这些“应激标签”的表达通过干扰素结合以及通过T细胞上的干扰素受体发出信号被抑制。如果由于受体的缺乏而阻止了信号的传输,那么细胞会大量表达这些应激分子。
尚不清楚人类是否具有相同的机制。然而,人类免疫系统用来保护T细胞避免NK细胞攻击的基本过程很可能是类似的。在一方面,研究人员揭示应激T细胞需要保护自己免受NK细胞攻击的机制。另一方面,这项发现形成了新的假设。例如,可以想到的是,缺乏干扰素受体的T细胞活化显示出它们为“应激的”,并因此杀死了。自身免疫反应性T细胞的活化过程中可能会出现这样的情况,例如,它通常发生在不存在高浓度的1型干扰素。Oxenius和她的团队有很浓厚的兴趣将在未来几年内测试这些令人兴奋的假设。
【中文名称】
自然杀伤细胞活性测定
【概述】
自然杀伤细胞(NK)介导天然免疫应答,它不依赖抗体和补体,即能直接杀伤靶细胞,如肿瘤细胞或受病毒感染的细胞等;此外,尚有免疫调节功能,也参与移植排斥反应和某些自身免疫病的发生发展。
【参考值】
51Cr释放法:自然释放率<10%~15%;自然杀伤率为47.6%~76.8%;51Cr利用率为6.5%~47.8%。酶释放法:细胞毒指数为27.5%~52.5%。流式细胞术法为13.8%±5.9%。
【临床意义】
NK细胞活性可作为判断机体抗肿瘤和抗病毒感染的指标之一。在血液系统肿瘤、实体瘤、免疫缺陷病、艾滋病和某些病毒感染患者,NK活性减低;宿主抗移植物反应者,NK活性升高。
圣祖德儿童研究医院的坎帕纳博士等人在新一期《血液》杂志网络版上发表论文说,此前用自然杀伤细胞治疗白血病的研究进展不快,主要是因为自然杀伤细胞对白血病细胞不敏感,也难以在实验室大量培养,而他们在这两个方面都取得了进展。
研究人员首先使用了含有各种免疫细胞的血样,将其与经过转基因处理的K562人类白血病细胞混合培养。这种白血病细胞经转基因处理后,表面带有“4-1BBL”和“IL-15”两种蛋白质。研究人员发现,转基因白血病细胞能刺激血样中自然杀伤细胞大量生长,其数量很快达到原先的1万倍,这使得自然杀伤细胞能提纯出来。
此后,研究人员对自然杀伤细胞进行转基因处理,使其表面生成能识别白血病细胞的受体蛋白。这种受体蛋白能与白血病细胞表面的蛋白质“CD19”结合,促使自然杀伤细胞溶解白血病细胞。
坎帕纳等人在论文中说,他们的方法能从少量血样中培养大量自然杀伤细胞,从而使自然杀伤细胞能实际应用于白血病治疗,这尤其适用于接受骨髓移植治疗的白血病患者。医生可以用骨髓捐献者的血样大量培养转基因自然杀伤细胞,然后在移植手术后注射到接受骨髓移植的患者体内,消灭残余的白血病细胞。
研究人员说,他们将很快对患有急性淋巴性白血病的儿童进行临床试验。如果试验显示积极效果,这种方法会成为白血病治疗的“利器”之一 。