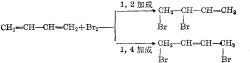
-
共轭双键 编辑
共轭双键体系即双键和单键交替的分子结构产生共轭效应。共轭效应的特点是化学键的极化作用可以沿共轭体系传递得很远。例如:共轭的结果是电子的离域,共轭体系内单键变短而双键变长,单双键长度差别缩小乃至消失。这样的体系比较稳定。如苯分子中六个碳-碳都是1.39A,而普通的碳-碳双键的键长为1.34A,碳-碳单键为1.48A。所以苯分子较环己烯分子更为稳定 。
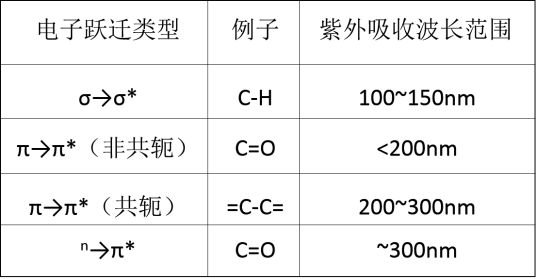
共轭双键是以C=C-C=C为基本单位,随着共轭度的增加,其紫外特性:最大吸收波长红移;如有荧光,其最大激发光波长红移,最大发射光波长红移;如有颜色的话,颜色逐步加深 。由于大π键各能级间的距离较近电子容易激发,所以吸收峰的波长就增加,生色作用大为加强。这种由于共轭双键中π→π*跃迁所产生的吸收带成为K吸收带。K吸收带的波长及强度与共轭体系的数目、位置、取代基的种类有关。
具有共轭双键的化合物,相间的π键与π键相互作用(π-π共轭效应),生成大π键。由于大π键各能级间的距离较近电子容易激发,所以吸收峰的波长就增加,生色作用大为加强。例如乙烯(孤立双键)的λmax=171nm(ε=15530L·mol-1·cm-1);而丁二烯(CH2=CH-CH=CH2)由于2个双键共轭,此时吸收蜂发生深色移动(λmax=217nm),吸收强度也显著增加(ε=21000L·mol-1·cm-1)。这种由于共轭双键中π→π*跃迁所产生的吸收带成为K吸收带。其特点是强度大,摩尔吸光系数εmax通常在10000~200000(>104)L·mol-1·cm-1之间;吸收峰位置(λmax)一般处在217~280nm范围内。K吸收带的波长及强度与共轭体系的数目、位置、取代基的种类有关。例如共轭双键愈多,深色移动愈显著,甚至产生颜色。据此可以判断共轭体系的存在情况,这是紫外吸收光谱的重要应用。
在该分子中,所有的原子处于同一个平面上,四个碳原子都以sp2杂化成键。形成了三个碳碳σ-键和六个碳氢σ-键。每个碳原子上的未杂化的p电子,垂直于平面,侧向交叠,形成一个π-π共轭体系 。
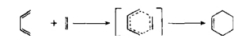
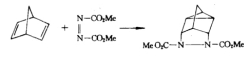
该反应的进行仅需光或热的作用,通常不受催化剂或溶剂极性的影响。运用轨道对称守恒原理可以使该反应的机理得到很好的阐明。
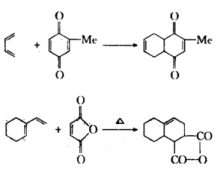
Diels-Alder反应常见的双烯体有脂肪族、脂环族共轭双键化合物以及某些芳香族类和杂环化合物等。常见的亲双烯体为连有醛基、羧基、酯基、硝基、氰基等吸电基的烯烃或炔烃,以及醌类等。此反应在高温下多为可逆反应,而且为放热反应。
具有供电基的双烯体与具有吸电基的亲双烯体都具有较大的反应活性,使得此反应多数发生于富电子的双烯体与缺电子的亲双烯体之间。例如,1,3-丁二烯与丙烯醛的反应几乎可以得到定量的产率。但是,取代基的碳原子数愈多,或取代基的数目增加都会使反应减缓。
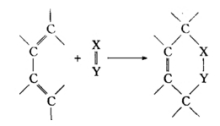
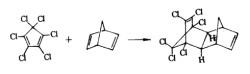
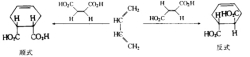
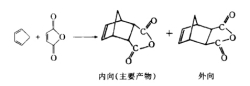
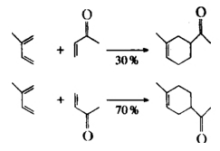
然而,此反应也可以在缺电子的双烯体与富电子的亲双烯体之间进行。据认为,为要进行此反应,双烯体与亲双烯体间应具有互补电子的性质。例如,艾氏剂(aldrin)的合成就是以缺电子的六氯环戊二烯为双烯体。Diels-Alder反应还可发生于分子内。某些双键空间位置相近的非共轭二烯也能与亲双烯试剂作用,这时三个π键转化为三个σ键而形成两个新的环。Diels-Alder反应具有高度的立体定向性,总是发生顺式加成。例如,1,3-丁二烯与顺丁烯二酸反应生成顺-1,2,3,6-四氢化苯二甲酸,而与反丁烯二酸反应则生成其相应的反式衍生物。该反应的这一立体化学特征表明,只有二烯绕C—C单键旋转能形成s-顺式构象才能发生此反应。因而下列两个化合物由于双键被环固定为s-反式构象,都不能与亲双烯体发生此反应Diels-Alder反应的另一立体化学特征为,当双烯体与亲双烯体都是环状化合物时,通常优先生成内向构型的加成产物。这是由于内向与外向两种构型相比,由底物形成过渡态所需的能量前者低于后者的缘故。此两构型产物的比例还受反应温度、溶剂极性等的影响。提高温度有利于外向构型产物的生成。不对称s-顺式构象的二烯与不对称亲双烯体之间的反应,因后者取向的不同可得到两种异构产物。一般的规律为:与1-取代丁二烯、2-取代丁二烯和1,3-二取代丁二烯反应得到的主要产物分别为邻位、对位和1,2,4-异构体。Diels-Alder反应广泛应用于环状有机物的合成,尤其在天然有机物和结构特殊化合物的合成中有着重要的价值。由呋喃与丁炔二酸二甲酯合成斑蝥素亦有赖于此反应。该反应亦用于定量测定有机物中的共轭双健 。