-
信号肽 编辑
中文名:信号肽
外文名:signalpeptide
类型:肽链
组成:氨基酸
提出人:Milstein
SRP活性能在体外由单个成分获得再生。其实有功能的SRP可由一种7SRNA和其它一些蛋白组装而成。像其它转运和跨膜蛋白一样,SRP普遍存在于真核生物中。
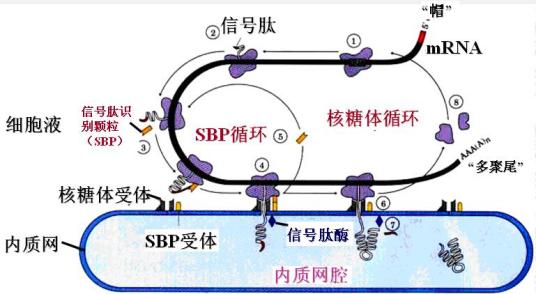
SRP和SRP受体二者的催化功能是将带有新生肽的核糖体转移到膜上。第一步是信号肽被SRP识别。然后SRP和其受体结合,核糖体结合到膜上。SRP受体在蛋白质转运中的作用是短暂的。当SRP和信号肽结合时,它阻止了翻译。蛋白合成停止。这是在新合成的多肽链长70aa左右时发生的。(这样25-30残基的信号肽伸在核糖体外面,相邻的约40个aa仍在核糖体中)。
当SRP与其受体结合时,SRP释放出信号肽,然后核糖体和膜上的其它成分(尚未鉴别出)结合,此时翻译得到恢复。当核糖体被传递到膜上时,SRP及其受体的作用已完成了,又进入新的循环。再自由地发动另一些新生肽和膜的结合。
此SRP7SRNA可分成两部分:5′端的100个碱基和3′端的45个碱基,这一段和AluRNA顺序密切相关,因此定义为Alu结构域(Aludomain)。RNA余下的部分由SRNA功能域(sRNADomain)构成。
RNP不同的部位对于靶蛋白具有相应三种功能。在体外用SRP的识别来研究每部分的功能。54KDA的蛋白只有一个分子,它不直接和RNA结合。而是和19kDa的蛋白结合,19KDa蛋白与RNA的两个未端结合。P54用来识别信号肽;P68/72双体结合于RNA的中心区域,它是用来识别SRP的受体及蛋白的越膜转运。P9/14二聚体结合在此RNA分子另一端的附近。它负责延伸制动。
SRP的受体是含有72Kda和30KDa两个亚基的二聚体。大亚基的N-端锚定在ER中,蛋白的大部分伸在胞液中,蛋白的此区域的大部分顺序与核结合蛋白相似,带有很多正电荷的aa,表明SRP受体识别SRP中的7SRNA。
为什么协同翻译的蛋白进入内皮网状系统,而翻译后转运的蛋白就要进入线粒体和叶绿体呢。还没有充分的证据来明确回答此问题,且在酵母中输入ER的蛋白却发生在翻译后转运,这使问题更为突出。两种过程对能量的需求是不同的。转运到线粒体或叶绿中需要一种电位差,而进入ER时需ATP。这并不意味着蛋白系统的作用涉及到能量的提供。核糖体的存在对于在协同翻译转运中维持蛋白进入膜中时的正确几何形状是需要的。