-
干细胞 编辑
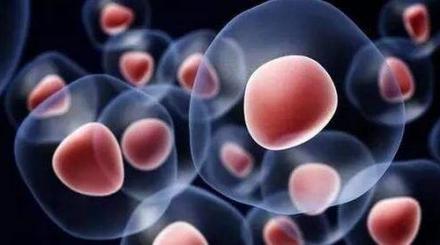
虽然在形态学和分子生物学水平上干细胞的结构意义能帮助定义干细胞,但是干细胞的定义仍必须是建立在功能性的基础上的。从功能上讲,干细胞是具有多向分化潜能、自我更新能力的细胞,是处于细胞系起源顶端的最原始细胞,在体内能够分化产生某种特定组织类型的细胞。对于单细胞来讲,对这个定义进行严格限制是很重要的。尤其是在复杂的器官中,为了区别干细胞和其他各种类型的祖细胞,对其进行功能上的区分可能更精确和必要。因为干细胞和祖细胞的定义是由其是否具有自我更新能力所决定的。干细胞一旦分化为祖细胞后就失去了自我更新的能力,出现对称性的有丝分裂,祖细胞的数量只有通过干细胞的增殖分化来补充,但是祖细胞仍然保持高度的增殖能力,就造血干祖细胞而言,各系造血过程中细胞的大量扩增主要依靠造血祖细胞的增殖。
在成体的器官中,干细胞可以通过不断分裂来修复组织,或者是像在哺乳动物脑组织中那样处于静止的状态。干细胞在其发育期间能够通过对称性地分裂以扩增它们的数量,或者通过非对称性分裂进行自我更新和产生更多不同分化类型的祖细胞。
科学地对干细胞进行分类有助于对干细胞概念及其生物学特性的准确把握和理解,可以采用以下几种方法对干细胞进行分类。
根据发育阶段分类
按照此种分类方式,干细胞可以分为胚胎干细胞和成体干细胞。
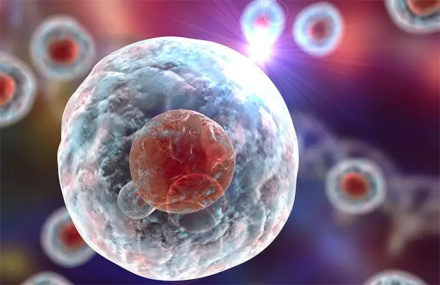
成体干细胞:成体干细胞是指存在于一种已经分化组织中的未分化细胞,这种细胞能够自我更新并且能够特化形成组成该类型组织的细胞。成体干细胞存在于机体的各种组织器官中。发现的成体干细胞主要有:造血干细胞、骨髓间充质干细胞、神经干细胞、肝干细胞、肌肉卫星细胞、皮肤表皮干细胞、肠上皮干细胞、视网膜干细胞、胰腺干细胞等。
根据不同的分化潜能分类
按照此种分类方式,干细胞可分为全能干细胞、多能干细胞、单能干细胞。
全能干细胞:具有自我更新和分化形成任何类型细胞的能力,有形成完整个体的分化潜能,如胚胎干细胞,具有与早期胚胎细胞相似的形态特征和很强的分化能力,可以无限增殖并分化成为全身200多种细胞类型,进一步形成机体的所有组织、器官。

单能干细胞(也称专能、偏能干细胞):常被用来描述在成体组织、器官中的一类细胞,意思是此类细胞只能向单一方向分化,产生一种类型的细胞。在许多已分化组织中的成体干细胞是典型的单能干细胞,在正常的情况下只能产生一种类型的细胞。如上皮组织基底层的干细胞、肌肉中的成肌细胞又叫卫星细胞。这种组织是处于一种稳定的自我更新的状态。然而,如果这种组织受到伤害并且需要多种类型的细胞来修复时,则需要激活多潜能干细胞来修复受伤的组织。

多向分化潜能和自我更新是干细胞的基本特点。具体来讲,干细胞具有以下一些生物学特点:
①属非终末分化细胞,终生保持未分化或低分化特征,缺乏分化标记。
②在机体的数目位置相对恒定。
③具有自我更新能力。
④能无限地分裂、增殖,可在较长时间内处于静止状态,干细胞可连续分裂几代。
⑤具有多向分化潜能,能分化为各种不同类型的组织细胞;也具有分化发育的可塑性,在特定环境下,能被诱导分化成在发育上无关的细胞类型,其分化受所处周围微环境的影响。
⑥分裂的慢周期性。
⑦干细胞通过两种方式生长,一种是对称分裂,形成两个相同的干细胞,另一种是非对称分裂方式,非对称分裂中一个保持亲代的特征,仍作为干细胞保留下来,另外一个子细胞不可逆的走向分化的终端成为功能专一的分化细胞。
尽管许多组织中都存在干细胞,但其数量很少,而且在显微镜下时,无法将它们与这些组织中的其他细胞清楚区分。因此,如何找到一种简单有效的方法,科学、准确地区分这类稀少的细胞,一直是科学家们不断探索的课题。
过去人们普遍采用的干细胞鉴别方法主要有以下两种:①利用干细胞的慢周期性,采用标记滞留细胞的分析方法来识别在体的静息干细胞。②利用干细胞的自我更新能力,观察其在体外培养时表现出的无限的增殖能力来识别离体的干细胞。但这两种方法应用时具有一定的限制性。

干细胞研究受到科学家和世人的广泛关注有其必然性,干细胞在生命科学的细胞修复、发育生物学、药物学等领域有着极为广阔的应用前景。
科学家们在经过长期的探索和努力之后,最终把目光落在干细胞上,生命体是通过干细胞的分裂来实现细胞更新及保证持续增长,干细胞的研究与应用将有可能使人类实现完美修复损伤组织和器官的梦想。多年来科学家们一直致力于寻找利用干细胞的复制和分化来取代受损细胞或组织的方法。这一点随着组织工程、胚胎工程、细胞工程、基因工程等各种生物技术的发展和干细胞生物学研究领域的突破而展现出无比广阔的前景。按照一定的目的在体外人工培养、分离干细胞已成为可能,利用干细胞构建各种细胞、组织、器官作为移植的来源将成为干细胞应用的主要方向。
发育生物学是生命科学的前沿领域,在最近几十年里,对发育生物学的某些基础领域有了较为深入的认识。但是发育生物学领域依然存在许多未解的问题,例如,一个单细胞——受精卵细胞是如何发育成复杂的组织、器官、系统乃至完整的有机个体?
生命最大的奥秘就是探讨一个受精卵如何发育成复杂的生物体,但是,由于受精卵植入子宫后的不可接近性,使人们对胚胎发育机制的探讨受到影响。而人胚胎干细胞系的建立将有助于我们探讨发育过程中的影响因素和调控机制。在对胚胎发育过程中关键性调控机制的研究中,胚胎干细胞无疑已成为一个重要的工具,例如,可以比较胚胎干细胞和不同时空的分化细胞之间的基因表达差异,研究参与胚胎发育与分化的分子机制。
作为疾病基因治疗的载体
干细胞是对疾病进行基因治疗的理想载体。造血干细胞具有自我更新、多向分化重建长期造血、采集和体外处理容易等特点。因此是基因治疗最理想的载体细胞之一,以此为基础的基因治疗,在重症免疫缺陷、遗传性疾病、恶性肿瘤、造血干细胞保护、AIDS等领域具有广阔的应用前景。
骨髓间充质干细胞易于外源基因的导入和表达,这种特点结合骨髓间充质干细胞的多向分化潜能,便使其可能成为一种理想的基因治疗的靶细胞。此外,人胚胎干细胞可以不断自我更新,经过遗传操作后依然能够稳定地在体外增殖,将其作为基因治疗的载体,将有可能解决基因治疗中所面临的用作载体的细胞在体外不能被稳定改造和传代的问题。胚胎干细胞的遗传改造将有可能被用于遗传性疾病的治疗领域。人们普遍关注的干细胞分离纯化技术的进步、基因转染效率的提高、基因转移载体(脂质体、逆转录病毒、腺病毒、腺相关病毒等)的不断改进及转基因细胞的扩增和定向诱导分化、新的目的基因的发现、目的基因转染后的稳定表达和调控等领域的深入研究将使得与干细胞相关的基因治疗更加有效和广泛地应用于临床。
体外整合外源基因,研究基因功能

药物筛选平台的建立,药理研究与新药开发
胚胎干细胞可以分化为多种细胞类型又能不断自我更新,这在药物研究领域具有广泛的用途。用于药物筛选的细胞都来源于动物或癌细胞这样非正常的人体细胞,而胚胎干细胞可以经过体外诱导,为人类提供各种组织类型的细胞,这为药物筛选、鉴定及其毒理的研究提供坚实的基础,并有助于人类疾病细胞模型的建立及新药开发。










