-
Caspase家族 编辑
由于这种特异性,使caspase能够高度选择性地切割某些蛋白质,这种切割只发生在少数(通常只有1个)位点上,主要是在结构域间的位点上,切割的结果或是活化某种蛋白,或使某种蛋白失活,但从不完全降解一种蛋白质。
 Caspase家族
Caspase家族
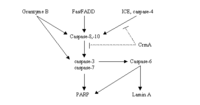
Caspase的研究源于线虫(C. elegans)细胞程序化死亡的研究。线虫在发育过程中,有131个细胞将进入程序化死亡;研究发现有11个基因与PCD有关,其中ced3和ced4基因是决定细胞凋亡所必需的,ced9基因抑制PCD。线虫细胞程序化死亡的研究促进了其他动物特别是哺乳类动物中细胞凋亡的研究。人们发现哺乳类细胞中存在着Ced3的同源物ICE(interleukin-1b convERTing enzyme),它催化白介素-1b的活化,即从其前体上将IL-1b切割下来。在大鼠成纤维细胞中过量表达ICE和Ced3都会引起细胞凋亡,表明了ICE和Ced3在结构和功能上的相似性;然而敲除ICE基因的小鼠其表现型正常,并未发现细胞凋亡发生明显改变。进一步的研究发现,另一个ICE成员,后来被称为apopain,CPP32或Yama的半胱氨酸蛋白酶,催化poly(ADP-ribose)Polymerase(PARP),即聚(ADP-核糖)聚合酶的裂解,结果导致细胞的凋亡,因而认为apopain执行着与线虫中的ced3相同的功能。Apopain被称为是“死亡酶”,而PARP被认为是“死亡底物”。Apopain/CPP32/Yama是在1995年由两个实验室分别同时报导,时间上只有两周之差。Ced4的哺乳类同源物则迟迟未能发现,直到1997年,才被证明是Apaf-1(即一种细胞凋亡蛋白酶活化因子apoptosis protease aCTivating factor)。而Ced 9的哺乳类对应物则较早地被证明是BCL-2,这一问题将在以后的部分述及。
现发现的哺乳动物细胞caspase家族成员共15种:
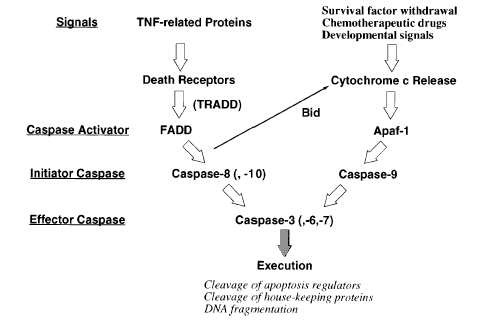
这些caspases中,caspase 1和caspase 11,以及可能还有caspase 4被认为不直接参与凋亡信号的转导,它们主要参与白介素前体的活化;而caspase 2,caspase 8,caspase 9和caspase 10参与细胞凋亡的起始;参与细胞凋亡执行的则是caspase 3,caspase 6和caspase 7,其中caspase 3和7具有相近的底物和抑制剂特异性,它们降解PARP,DFF-45(DNA fragmentation factor-45),导致DNA修复的抑制并启动DNA的降解。而caspase-6的底物是lamin A和keratin 18,它们的降解导致核纤层和细胞骨架的崩解。
细胞中合成的caspase以无活性的酶原状态存在,以后经活化方能执行其功能。
一般的蛋白酶活化时,只是将N-末端的肽段切除,而caspase的活化则需在两个亚基的连接区的天冬氨酸位点进行切割,结果产生了由两个亚基组成的异二聚体,此即具有活性的酶。通常N-末端的肽在活化时也被除去,但对于caspase 7是否去除N-末端肽对活性无影响。认为细胞凋亡的起始者(caspase 2,8,9和10)和执行者(caspase 3,6和7)之间存在着上下游关系,即起始者活化执行者。
凋亡起始者(caspase 2和10)的活化属于同性活化(Homo activation)。caspase 8和10含有串联重复的“死亡效应子”结构域(death effECTor domain,DED),而caspase 2和9则含有不同但类似的caspase募集结构域(caspase recruitment domain CARD),这两种结构域是募召caspase 2,8和10所必需的。