-
电泳图谱 编辑
带电粒子在电场的作用下,向着与其电性相反的电极移动的现象,称为电泳。利用带电粒子在电场中移动速度不同,对混合物各组份进行分离、纯化和测定的技术称为电泳技术。可分离的样品即可以是大分子的蛋白质、多糖、核酸,也可以是小分子的氨基酸,核苷等。电泳方式差别很大.但基本原理是一致的,即:待分离样品中各种分子在同一pH下带电性质和带电量以及分子本身大小、形状等性质的差异,使带电分子在电场中产生不同的迁移速度,从而实现对样品分离、鉴定或提纯。
不同种类的电泳实现方式和技术关键各不相同,纷繁复杂:尚没有任何一种分类体系可以做到不重复的涵盖所有电泳方式。综合考虑支持物类型、电泳原理、用途等因素的系统分类方法简单清晰,而且主要的电泳种类都能在该体系中找到自己的位置。
按是否使用支持物分为
无支持物的电泳技术
此类电泳也称自由电泳。电泳方式是直接将待测样品溶于适当的缓冲液中,在缓冲液两端通电,形成电场,带点粒子在溶液中自由泳动达到分离的效果。包括Tise-leas式微量电泳、显微电泳、等电聚焦电泳、等速电泳及密度梯度电泳等。自由电泳由于电泳仪构造复杂、体积庞大,操作要求严格,价格昂贵等原因,发展比较缓慢。往往只有当其他技术难以满足分析、分离要求时才会选择自由电泳,如等电聚焦电泳是准确测量蛋白质等电点的无可替代的方法。
有支持体的电泳技术
电泳方式是选择滤纸、凝胶等适当物质做支持物,将支持物两端或全部浸入缓冲液中,并达到缓冲体系平衡,在支持物上加样,缓冲液两端加电压,形成电场从而实现电泳效果。带点粒子本身性质和支持物口径大小等因素共同决定其泳动的最终位置。电泳结果表现为不同组份形成相隔离的区带,故此类电泳又称区带电泳,包括纸电泳,醋酸纤维薄膜电泳,薄层电泳,粉末电泳(支持物有:淀粉,纤维素粉,玻璃粉等),凝胶电泳(聚丙烯酰凝胶,硅胶,琼脂(糖)凝胶)。区带电泳种类繁多,应用十分广泛,发展迅速是生物分析技术中的热点之一。
区带电泳根据支持物装置和电泳方向不同分为
(2)垂直柱式电泳:装置为玻璃管,垂直方向电泳。
(3)垂直板式电泳:装置为玻璃板,垂直方向电泳。
(4)毛细管区带电泳:以毛细管为分离通道。
电泳迁移率
带电粒子在电泳过程中得以分离,依赖于不同粒子在同一电场强度下泳动的速度不同。带电粒子在电场中的移动速度,用迁移率(或称泳动度,mobility,μ)表示。迁移率的定义为带电粒子在单位电场强度下的泳动速度。
带电粒子在电场中的泳动速度,由一对相反的作用力一电场力和阻力决定。其中
式2中F——电场力(牛顿);q——离子的净电荷(库仑);E——电场强度(伏特/米):式3中
当这两个力相等时,泳动速度恒定,与F成正比,与
影响电泳的主要因素
带电粒子迁移率不同是电泳分离的基础,因此影响迁移率的所有因素都是影响电泳的因素。由式5可见,这些因素即包括带电粒子本身的性质,也包括电泳体系的条件,甚至不同类型的电泳主要影响因素也不相同。下面简单讨论一下这些条件。
1.带电粒子性质
带电粒子所带的静电荷量、粒子大小、形状等性质对泳动速度有明显影响。一般情况下,粒子所带净电荷量越大,直径越小,形状越接近球形,其在电场中的泳动速度就越快:反之,则越慢。
2.电场强度
电场强度是每厘米的电位降,也称电位梯度。由式1可见,电场强度越大,电泳速度越快。反之,则越慢。根据电场强度大小,电泳可分为常压电泳和高压电泳。前者电场强度为2~10V/cm,后者为20~00V/cm。用高压电泳分离样品比常压电泳用时短。应该指出,并不是电场强度越大越有利于电泳分离。电场强度的增大,通过介质的电流强度随之增大,将造成电泳过程产生的热量增大,进而影响电泳效果。
3.缓冲体系性质
(1)PH值
缓冲液的pH值决定带电粒子的解离程度,及其带净电荷的量。电泳速度因此受很大影响。对两性分子而言,pH值还决定带电粒子的电性,进而影响其电泳方向。一般说来,缓冲液pH值离两性分子等电点愈远,其带净电荷量愈大,泳动速度就愈快。反之,则愈慢。
(2)离子强度
缓冲液的离子强度通常保持在0.02~0.2之间较合适。离子强度过低,则体系缓冲能力差,往往会因电泳过程中溶液pH值变化而影响泳动速度的稳定性。离子强度过高,则会因静电引力作用降低颗粒的泳动速度。
(3)黏度
由式5可见,缓冲体系液黏度与迁移率成反比。因此,溶液黏度越大电泳速度越小,反之,越大。
4.电渗
电渗指在电场中液体对固体支持物的相对移动,如滤纸表面带负电,带正电的水层便会向负极移动。当支持物不是绝对惰性物质时,电渗现象与电泳同时存在。电渗与电泳方向一致时,就会产生类似顺风游泳的情况,加快电泳速度;反之,则降低颗粒的泳动速度。(图1)
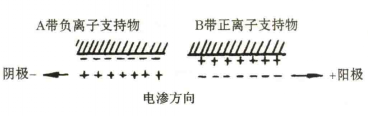 图1 电渗示意图
图1 电渗示意图
5.焦耳热
电泳过程中释放出的热量与电流的平方成正比。当电场强度增大或电极缓冲液中离子强度增高时,电流会随着增大。如果散热系统无法满足需要,电泳体系温度就会有较大升高。这不仅降低分辨率,而且在严重时会烧断滤纸或熔化琼脂糖凝胶支持物。
6.支持介质的筛孔大小
支持介质的筛孔大小取决于支持介质性质和浓度。实验时需根据电泳分析、分离的目的慎重选择筛孔的大小。筛孔大的介质中,电泳速度快,分辨率较低。反之,则泳动速度慢,分辨率较高。
手工电泳装置
1.电泳槽
电泳槽是电泳系统的核心部分。一般由装有铂金丝电极的主槽和胶室支架组成。主槽中注入缓冲液,并连接电源的正、负极;胶室支架放电泳支持物,与主槽电极缓冲液接触或直接浸没入缓冲液中。根据实验设计可分为管式电泳槽、垂直板电泳槽、水平板电泳槽等类型。
 图2垂直板式电泳槽
图2垂直板式电泳槽
 图3平板式电泳槽
图3平板式电泳槽
2.电 源
电源的作用是建立电泳电场。而电场与电压有关,一般可分为:常压电泳:100~500V,场强1~10V/cm,分离时间较长;高压电泳:500~10kV,场强20~200V/cm,分离时间短。也可根据功率输出特点将电源分为稳流、稳压和稳功率三种类型。
3.外循环恒温系统
高电压会产生高热,需冷却。常压电泳一般只要将电泳槽上配备的冷凝水上管接通自来水,下管接实验室水槽即可。高压或分离条件较苛刻的电泳则需配备专门的外循环恒温系统。
4.电泳区带分析装置
电泳分离后将电泳区带切下,再用洗脱液洗脱下来,可用分光光度计测定每一区带组分浓度。也可用凝胶成像分析系统直接对电泳区带进行密度扫描,从而得出相对百分比,并可绘制出曲线图,计算出相对面积。
全自动电泳分析仪
从电泳技术问世起,效果最优化和操作简便化就是科研工作者的不懈追求。随着电泳技术的发展和进步,各种先进电泳仪的不断涌现:1990年以来Pharmacia LKB公司、法国Sebia、美国Helena等纷纷推出全自动电泳系统。下面以Helena公司的SPIFE3000全自动血浆蛋白质、血清免疫固定电泳(IFE)、碱性磷酸酶、尿蛋白、胆固醇、乳酸脱氢酶等:系统由计算机、扫描仪、打印机和主机组成。操作者根据需要,预先将样品数量、凝胶性质、电泳时间等参数编入程序,系统可自动完成点样、电泳、倾倒和涂抹试剂、染色、固定、脱色和干燥等操作,并可自动扫描,完成结果分析和输出。
 图4 SPIFE3000全自动电泳仪
图4 SPIFE3000全自动电泳仪
区带电泳(zone electrophoresis)是有支持介质的电泳,样品中各组份在支持介质上分离成若干区带,是一种在生物测试领域中应用最广泛的电泳方法。区带电泳因所用支持介质的种类和电泳方式等不同,在科研实践中的应用价值也各有差异,电泳条件和介质的选择是电泳成败的关键。
基本原理
区带电泳常用来分离分析DNA、蛋白质等生物大分子。选择适当的在pH值,使pH>pl,则待分离组分带负电将向正极移动。其迁移率是电场作用、待测组分性质、固相介质吸附作用等各种影响因素综合的结果。电泳后,将吸附了待测组分的介质浸于适当染料中使之结合,经干燥处理,光密度计扫描,以各峰面积积分结果计算各组分含量。
介质选择
区带电泳是依靠带电粒子在电泳介质上泳动而实现分离的手段。电泳介质的选择极大的影响着电泳的结果。在选择凝胶介质时,一般需从影响电泳迁移率的诸因素、技术可行性、资源最优化、待测组分性质等方面综合考虑。常用介质包括以下几种:
(一)滤纸
区带电泳发展之初,以湿润的滤纸作为电泳介质。随后,纸层析技术出现,电泳和层析技术的结合极大的扩展了滤纸电泳的应用范围。纸电泳具有设备简单、操作方便的优点。同时也存在着电渗现象严重,操作时间长、分辨率较差等劣势。已逐步被许多新型材料取代。
(二)醋酸纤维素膜
醋酸纤维素是由纤维素的羟基经乙酰化而成纤维素醋酸酯。醋酸纤维素膜对蛋白质样品的吸附作用极小,有利于避免“拖尾”现象,是蛋白质电泳的常用介质之一。醋酸纤维素膜吸水性小,有利于节约缓冲液,加快电泳速度。醋酸纤维素膜的电泳图谱经透明液处理后可使膜质透明化,有利于测定和长期保存。其缺点在于有电渗作用。
(三)琼脂糖凝胶
琼脂糖主要成分是一种直链多糖,微波或水浴中加热可溶解与水中,冷却后依靠糖链之间的次级链如氢键来维持网状结构,网状结构的疏密与琼脂糖的浓度相关。琼脂糖亲水性强,且不含带电荷的基团,极大减少了待测样品变性和吸附。主要用于核酸分析。
(四)聚丙烯酰胺
聚丙烯酰胺是丙烯酰胺单体和甲叉双丙烯酰胺交联剂按一定比例混合,在催化剂(如过硫酸铵)作用下聚合而成的交叉网状结构的凝胶,使其产生分子筛效应。凝胶孔径大小可以通过制备时所使用的浓度和交联度控制。聚丙烯酰胺凝胶的优点是兼有电泳介质及分子筛的功能,大大提高了分离能力,是分辨能力最高的电泳介质。
菌体蛋白质电泳
疫霉菌的分类鉴定仍以形态特征为主要依据。但是,由于疫霉菌形态变异较大,一些分类依据不稳定,因而有时依据形态难以鉴定。已经证明,同种疫毒菌菌株间的菌体可溶性蛋白质电泳图谱相似,主要蛋白带型相同。应用这一技术,已成功地确定了一些依据形态特征难以鉴定的疫霉菌株的分类地位。
一、蛋白质样品的制备
将新鲜培养的菌丝块(大小约2×2mm)数块接种于盛有适合疫霉菌生长的培养液的平底烧瓶中(每个250ml容量的平底烧瓶装150ml培养液)。在适温、黑暗条件下静置培养7天左右,用干净纱布滤出菌丝体。将菌丝丛中的培养基小块去掉,菌丝体用25%乙醇冲洗,再用蒸馏水反复冲洗3~4 次,在双层纱布中挤去多余的水份。收集冲洗后的菌丝并称湿重,按1:1(W/V) 加入pH6的磷酸缓冲液(0.2M Na2HPO4 123ml与0.2M NaH2PO4877ml 混合配制),冰冻过夜。将冰冻后的菌丝体置于研砵中,加入少量石英砂,在冰浴下充分研磨成糊状。研磨后的菌丝液在18000转/分、4℃下离心1小时,倾出上清液。在上清液中加入10~15%的甘油或蔗糖(以防止加样后样品在电极缓冲液中漂浮),即为菌体可溶性蛋白质电泳样品。
确定电泳样品中蛋白质含量:将标准酪蛋白溶解在pH6的磷酸缓冲液中,配成系列浓度。用紫外分光光度计在280nm波长下测定各浓度的OD值,画出标准曲线。在相同光波长下测定电泳样品的OD值,根据该OD值从标准曲线上查找出电泳样品的蛋白质含量。
二、聚丙烯酰胺凝胶垂直平板电泳
(一) 电泳贮备液
1号液::1N HCI 48ml,三羟甲基氨基甲烷(Tris)36.6g,四甲基乙二胺(TEMED)0.5ml,用蒸馏水定容至100ml,pH8.9。
2号液:1N HCl 48ml,三羟甲基氨基甲烷5.98g,四甲基乙二胺0.7ml,用蒸馏水定容至100ml,pH6.7。
3号液:丙烯酰胺28.0g,
4 号液:丙烯酰胺10.0g,
5 号液:过硫酸铵0.14g,用蒸馏水定容至100ml。
上述1、2、3和4号液配制后盛于棕色瓶中于4℃下保存,可贮藏1~2个月,但5号液配制后冷藏时间不超过1星期。
电极缓冲液:三羟甲基氨基甲烷6.0g,甘氨酸28.8g,用蒸馏水定容至1000ml。使用前稀释10倍。
(二) 制胶
取1号、3号液、蒸馏水和5号液按2:4:8:8的比例混合,加入垂直电泳槽制成分离胶。待分离胶凝固后,取2 号、4号液、蒸馏水和5号液按1:2:1:4比例混合,在电泳槽上插入加样梳,灌入依缩胶。待浓缩胶凝固后,拔出加样梳,并吸去加样孔中多余的水分。
(三)电泳
用微量加样器在各加杆孔中加入电泳样品,每孔的蛋白质加样量为100μg左右。在电泳槽中加入电极缓冲液并滴加2滴1%溴酚兰指示前沿线,电泳。开始时电流强度用30mA,待样本进入分离胶时调至50mA。电泳过程中,将电泳槽置4℃冰箱中进行。
三、染色与脱色
电泳结束后,将凝胶薄片取下,置于考马斯亮兰R250染色液(考马斯亮兰R250 2.5g,三氯醋酸200ml,加水至1000ml)中染色24小时。倾去染色液,用7%醋酸溶液脱色至胶片背景近于无色。胶片可供拍照、绘图和结果分析用。
四、电泳图谱绘制与分析
根据聚丙烯酰胺凝胶薄片上蛋白质电泳带的粗细、深浅和迁移率,绘制电泳图谱,并计算相似率。
(一)迁移率计算
迁移率=(起点至蛋白带的距离/起点至指示剂前沿线的距离)×100%.
其中起点系指加样一端分离胶的起点线,指示剂前沿线指电泳结束时溴酚兰指示剂在胶板另一端形成的蓝色线。例如,某蛋白带的迁移距离是3cm,起点至指示剂前沿线距离是10cm,则该蛋白带的迁移率为0.3。比较两个菌株间的相似性时,迁移率差异小于0.03的两条蛋白带被视为相似的蛋白带。
(二)菌株间的相似率计算
相似率=(两菌株相似蛋白带的数目/两菌株蛋白带的总数)×100%.
例如,两个菌株间迁移率相似的蛋白带有5对(10条),两菌株蛋白带总数为15条,则这两个菌株的相似率为67。相似率越高,菌株间的相似性越大。通常,同一个疫霉种菌株间的可溶性菌体蛋白质电泳图谱相似率在75~100之间。










