-
托特罗定 编辑
基本信息
中文名称:托特罗定
中文别名:氘代托特罗定-d14;-2--1-苯丙基]-4-甲基苯酚;(R)-2--4-甲基苯酚;6-?-2--4-甲基苯酚;
英文名称:tolterodine
英文别名:Tolterodine L-tartrate;TOLTERODINE TARTRATE;
CAS号:124937-51-5
分子式:C22H31NO
分子量:325.48800
精确质量:325.24100
PSA:23.47000
LogP:5.34140
物化性质
密度:0.893g/mLat 25°C(lit.)
沸点:66-67°C10mm Hg(lit.)
闪点:154°F
折射率:n20/D 1.4536(lit.)
蒸汽压:2.02E-09mmHg at 25°C
安全信息
符号:GHS06;GHS08
信号词:危险
危害声明:H301; H361
警示性声明:P281; P301 + P310
危险品运输编码:1987
WGK Germany:2
危险类别码:R22
安全说明:S36/37/39
危险品标志:Xn; Xi
毒理学数据
酒石酸托特罗定:雄性小鼠静脉注射LD50:10~20mg/kg
分子结构数据
1、 摩尔折射率:98.34
2、 摩尔体积(cm/mol):307.8
3、 等张比容(90.2K):768.5
4、 表面张力(dyne/cm):38.8
5、 极化率(10-24cm3):38.98
合成方法
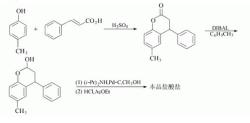
反式内桂酸(100g,675mmol)加到反应瓶中,加入预热到60℃的对甲苯酚(76.6g,708mmol),然后加入浓硫酸(13.0ml,243mmol)。加毕,马上加热到122.5℃,然后在120~125℃搅拌至反应完全,约6h。冷却至100℃,倾入预热过的分液漏斗。分出下层酸层,加入280ml甲苯、50ml水和10ml47%的碳酸钾溶液。如有需要,可用47%的碳酸钾将水层的狆犎值调至5~8。分出有机层,用50ml水洗,减压浓缩至大约150ml。加入350ml异丙醇,浓缩至剩350ml。加入150ml异丙醇,浓缩至剩350ml。再加入150ml异丙醇,再浓缩至剩350ml。在快速搅拌下冷却至30~40℃,使形成结晶,并继续搅拌。然后冷却至0~5℃,并保持1h。过滤收集结晶,用0~5℃的200ml异丙醇分批洗,如最终的洗液仍有颜色,则继续洗,直至洗液无色。在60℃和减压下干燥,得3,4-二氢-6-甲基-4-苯基-2H-苯并吡喃-2-酮,熔点83~85℃。3,4-二氢-6-甲基-4--苯基-2H-苯并吡-2-酮(100.0g,420.2mmol)加到500ml甲苯中,冷至-21℃和在氮气保护下,在2h中缓慢加入二异丁基氢铝的甲苯溶液(DIBAL,1.5mol/L,290ml,435mmol),并维持反应温度为-20~-25℃。当反应完全后,在-20~-25℃加入45ml乙酸乙酯。然后加入500ml
23%的柠檬酸,所成溶液在45~50℃搅拌1h(或在20~25℃搅拌过夜)。分出有机层,用2×300ml水洗后,减压浓缩至剩250ml.加入500ml甲醇,再浓缩至250ml,重复操作。然后浓缩至油状物,静置结晶,得到3,4-二氢-6-甲基-4-苯基-2H-苯并吡喃-2-醇,直接用于下步反应。100g3,4-二氢-6-甲基-4-苯基-2H-苯并吡喃-2-醇在500ml醇的溶液,在氮气保护下,缓慢加入22g5%的钯-炭(1-5mmol)。加入二异丙胺(147.0ml,1.05mol),在0.32~0.35MPa和48℃下加氢至完全。通常反应约10h,也可反应过夜。冷却,移出反应器,再用150ml甲醇清洗反应器。清洗液和反应液合并,过滤,滤液浓缩,再加入乙酸乙酯至700ml,加热至55℃。在15mol中,加入52.5ml浓盐酸。缓慢冷却至-15~-20℃,并保持1h。过滤收集固体,真空干燥过夜,得盐酸托特罗定,熔点199~201℃。
用途
1mg,2mg;
酒石酸托特罗定胶囊:2mg;
酒石酸托特罗定缓释胶囊:2mg,4mg。
托特罗定口服后吸收迅速,用于治疗尿失禁1h可起效,持续时间约5h。口服即释剂的达峰时间为1~3h,口服缓释剂的达峰时间为2~6h。口服2mg,达峰时间约2.5h,血药浓度峰值(cmax)为2.5μg/L,曲线下面积(AUC)为11.8(μg·h)/L。在1~4mg剂量范围内,托特罗定的血药浓度峰值及曲线下面积与剂量呈线性关系。托特罗定口服生物利用度为77%,因首关消除显著,绝对生物利用度为30%~40%(范围为10%~74%)。进食对托特罗定吸收影响较小。托特罗定蛋白结合率较高,游离药物浓度平均为(3.7±0.13)%,分布容积约113L。主要在肝脏经细胞色素P450(CYP)2D6同工酶代谢,生成具有托特罗定相似药理学特性的5-羟甲基代谢物(DD01),进一步的代谢将产生5-羧酸和N-脱烷基5-羧酸代谢物。约77%药物经肾脏排泄,约17%药物经粪便排出,尚不清楚托特罗定是否经人乳分泌。原形药物的排泄率不到给药量的1%,5%~14%以活性DD01回收,尿液中回收的羧基代谢物和去烷基代谢物分别为51%和29%。静脉给药的总体清除率为9.5~45L/h,口服给药的总体清除率为5.7L/(kg·h)。托特罗定消除半衰期为2~3h,DD01的消除半衰期为3~4h。给药24h内大部分药物自人体排出,重复给药无蓄积性。
用于膀胱过度兴奋引起的尿频、尿急或紧迫性尿失禁等症状的治疗。
1.(1)有膀胱出口梗阻等尿潴留风险者。(2)有幽门狭窄等胃潴留风险者。(3)肝功能不全者。(4)肾功能不全者。(5)自主性神经疾病患者。(6)食管裂孔疝患者。
2.药物对儿童的影响 儿童用药的安全性和有效性尚未确定,不推荐儿童使用托特罗定。
3.药物对妊娠的影响 动物实验表明大剂量药物可引起胎仔体重减轻,增加死胎及畸胎的发生率,孕妇应慎用托特罗定。美国药品和食品管理局(FDA)对托特罗定的妊娠安全性分级为C级。
4.药物对哺乳的影响 动物实验表明托特罗定可经老鼠乳汁排泄,尚不清楚是否经人乳分泌。哺乳妇女用药应暂停哺乳或避免服用托特罗定。
5.用药前后及用药时应当检查或监测 (1)膀胱内压。(2)常规血液生化学检查。(3)心率及收缩压(尤其是有心血管疾患者)。
6.托特罗定可致视力模糊,影响反应时间,用药期间驾驶车辆、操作机器、进行危险作业者应引起注意。
7.药物过量所致严重不良反应包括眼调节失调和排尿困难等,可予洗胃及活性炭治疗。药物过量可予对症处理:(1)严重的中枢抗胆碱作用(如幻觉、严重的兴奋状态),可予毒扁豆碱治疗。(2)惊厥或明显的兴奋状态,可予苯二氮卓类药物治疗。(3)呼吸功能失调可予人工呼吸。(4)心动过速时可予β-肾上腺素受体阻断药。(5)尿潴留时可予插导尿管。(6)瞳孔放大时可予毛果芸香碱滴眼,或将病人置于暗室。
8.用药时间超过6个月者应考虑是否需进一步治疗。
孕妇及哺乳期妇女用药:
孕妇慎用本品,哺乳期间服用本品应停止哺乳。
儿童用药:
尚无儿童用药经验,不推荐儿童使用。
1.(1)口干。(2)胃肠道:消化不良、便秘、腹痛、胀气、呕吐。(3)眼:眼干、视物模糊。(4)皮肤:皮肤干燥。(5)精神神经系统:嗜睡、神经过敏、感觉异常、头痛。
1.成人常规剂量:口服给药,初始剂量为一次2mg,一天2次,视病人反应及耐受程度,可减量至一次1mg,一天2次。
2.成人肝功能不全时剂量:肝功能损害者,推荐剂量为一次1mg,一天2次。
3.成人其他疾病时剂量:正在服用CYP3A4抑制剂者,推荐剂量为一次1mg,一天2次。
1.托特罗定与CYP3A4强效抑制剂,如大环内酯类抗生素(红霉素、克拉霉素)、抗真菌药物(酮康唑、咪康唑、伊曲康唑)及蛋白酶抑制剂(环孢素、长春碱)等合用,可能抑制CYP3A4介导的托特罗定代谢活性,致代谢功能不良患者的血药浓度增加,潜在药物过量的风险,故不建议两者合用,必须合用时应注意调整剂量。
2.健康个体合用托特罗定与华法林未见明显相互作用,但有两者合用引起国际标准化比值(INR)升高的报道,出血风险增加,可能与竞争由CYP3A4介导的代谢有关,合用时应注意调整剂量。
3.氟西汀可减少托特罗定的代谢,使托特罗定曲线下面积增加,活性代谢物的血药浓度峰值及曲线下面积下降,但临床意义不明显,两者合用无需调整剂量。